Сосудистая стенка при гипертонии
Нарушение функции проницаемости и метаболизма в сосудистых стенках, несомненно, связано с изменениями афферентной импульсации, поступающей с ангиорецепторов в центральные регулирующие сосудистый тонус нервные приборы. По-видимому, возникающая гипоксия и нарушенная афферентная импульсация ведут не только к структурным изменениям, но и к расстройству синтетических процессов в сосудистой стенке.
Реальность этих механизмов показана нашими опытами, когда условнорефлекторные изменения общего уровня артериального давления сопровождаются немедленным увеличением концентрации прессорпых веществ в крови, устанавливаемой спектральным анализом.
Отсюда понятно, что при длительном нарушении координационных функций между центральными нервными регулирующими сосудистый тонус приборами и периферическими сосудами возникают патологические рефлекторные связи, базирующиеся на измененной сосудистой реактивности, нарушенной афферентной импульсации с соответствующей выработкой прессорных веществ длительного действия.
Фактор повышенного давления изменяет не только внутрисосудистое давление, но и внутри-стенное, не говоря уже о механическом сдавлении vasa vasorum; следовательно, возникает нарушение кровоснабжения и питания сосудистой стенки, расстройство метаболизма и реактивности ее нервных приборов.
Таким образом, схематически можно представить порочный круг условий, создающихся, например, в связи с нарушением кровообращения в сосудах головного мозга. Несомненно, что все события, возникающие в последующем, могут реализоваться лишь в случае временного выключения многочисленных компенсаторных механизмов, могущих свести на нет возникшие нарушения кровообращения в головном мозгу. В этом случае может возникнуть цепь реакций, теснейшим образом последовательно связанных друг с другом, вызывающих и осложняющих друг друга.
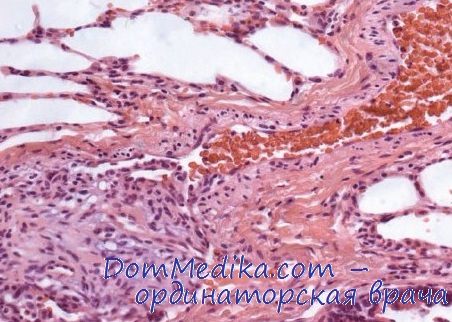
Реактивность кровеносных сосудов при стенокардии и инфаркте миокарда
Реактивность кровеносных сосудов при стенокардии и инфаркте миокарда в настоящее время представляет интерес для кардиологов-экспериментаторов и клиницистов. Этот вопрос является одним из главных среди других аспектов патогенеза коронарной недостаточности.
Оценка и понимание измененной реактивности сосудов организма при стенокардии и инфаркте миокарда возможны при тщательном учете многочисленных условий и связей, от которых этот процесс зависит. В данной главе мы ограничимся рассмотрением основных моментов и патофизиологических условий, с которыми связана сосудистая реактивность при коронарной недостаточности различного происхождения.
Измененная реактивность сосудов является важным фактором патогенеза или становится им по мере развития начавшегося сердечно-сосудистого заболевания. Для иллюстрации этого положения возникает необходимость анализа как литературных, так и собственных экспериментальных данных по следующим главным вопросам. Мы полагаем, что к ним относятся: структурные и ультраструктурные измепения, нарушения иннервации сосудов и миокарда, развитие коллатералей и новообразование сосудов в сердце и вне его.
Подлежат рассмотрению вопросы различных рефлекторных влияний на сосуды сердца и с сердца на остальную часть сосудистой системы, сопряженные с ними процессы ферментативных изменений на клеточном и молекулярном уровне. Важным вопросом является влияние различных степеней острой и хронической гипоксии и нарушения при ней нейро-гуморальной регуляции сердечно-сосудистой системы.
Исследователи все больше и быстрее подходят к стиранию граней между функциональными, метаболическими и структурными изменениями.
— Читать «Иннервация сердечных сосудов. Рецепторы коронарных сосудов»
Оглавление темы «Реактивность коронарных сосудов»:
- Влияние эуфиллина и строфантина на сердце при гипертонии. Гипоталамус при гипертонии
- Сосудистая стенка при гипертонии. Реактивность кровеносных сосудов при стенокардии и инфаркте миокарда
- Иннервация сердечных сосудов. Рецепторы коронарных сосудов
- Вены Тебезия. Анастомозы между коронарными сосудами
- Кровоснабжение рубца после инфаркта миокарда. Анастомозы коронарных сосудов при инфаркте миокарда
- Причины коронарной недостаточности. Механизмы развития стенокардии и инфаркта миокарда
- Атеросклероз как причина коронарной недостаточности. Физическая и психическая перегрузка как причина инфаркта миокарда
- Травма как причина инфаркта миокарда. Коронарная недостаточность при травме черепа и мозга
- Инфаркт миокарда при физическом перенапряжении. Безболевые формы стенокардии
- Адаптация миокарда к инфаркту миокарда. Иммунитет в постинфарктный период
Источник
Сосуды при гипертонии имеют характерные изменения, которые можно определить как при осмотре, так и при обследовании.
При простом ощупывании артерий создается определенное впечатление не только о повышенном давлении (внутриартериальном), но и об усиленном напряжении самих артериальных стенок (сосуд обычно хорошо прощупывается вне пульсовой волны). Поэтому можно было бы думать о наличии в них гиперпластических изменений.
Морфологические исследования артерий в этом направлении дали, однако, разноречивые результаты. Гипертоническое утолщение мелких артерий действительно наблюдается, но оно относится только к внутренней оболочке. Гиперплазия интимы мелких артерий отмечена особенно в сосудах почек, головного мозга, миокарда, селезенки; в других органах она встречается гораздо реже и в значительно менее выраженной степени.
Этот процесс захватывает эластическую и коллагеновую ткани внутренней оболочки. Что же касается мышечной оболочки артерий, то против ожидания (по крайней мере со стороны клиницистов) гиперплазия и гипертрофия средней оболочки при гипертонической болезни, судя поданным упомянутых выше авторов, не обнаруживаются; скорее приходится наблюдать ту или иную степень ее атрофии.
Правда, С. С. Вайль находил гипертрофию мышечной оболочки артерий и артериол в ряде органов — мозге, сердце, почках. Он отмечал ее неравномерный характер, что соответствует и впечатлениям клиницистов, ощупывающих часто четкообразные уплотнения артерий. Гипертрофия мышечного слоя развивается пропорционально степени и длительности гипертонии.
Гиперпластические и гипертрофические изменения сосудов при гипертонии объясняются нейрогенным повышением тонуса гладких мышечных элементов сосудов и большим реактивным напряжением сосудистых стенок под воздействием повышенного внутриартериального давления. Естественно, что в дальнейшем выступают на сцену уже иные — альтеративные изменения в сосудах при гипертонии.
Эти изменения сосудов при гипертонии заключаются прежде всего в нарушении проницаемости сосудистых стенок. В наибольшей мере они изучены Б. Н. Могильницким. За пределы сосудистого русла зависимо от степени проницаемости сосудистых стенок выходят различные белки: как мелкодисперсные (альбумины), так и грубодисперсные (глобулины, фибриноген). Белковые массы — негомогенные, зернисто-нитчатого рыхлого строения — содержат фибрин. Обычно они проникают не только во внутреннюю сосудистую оболочку, но и глубже; отложение их в сосудах некоторых органов, особенно почек, часто приводит к значительным структурным изменениям сосудов, даже к некрозам их стенок.
В результате нарушений сосудистой проницаемости при гипертонической болезни развивается плазматическое пропитывание стенок сосудов, отложение в них белковых гиалиновых масс. Эти «плазморрагии» в дальнейшем приводят к дистрофическим и некротическим изменениям стенок сосудов, а затем и к склерозу стенок.
Плазматическое пропитывание стенок мелких сосудов при гипертонии в наибольшей мере наблюдается при быстро текущих формах гипертонической болезни. Вот почему оно обычно обнаруживается при злокачественном варианте ее течения.
Плазматическая инфильтрация сопровождается развитием реактивных явлений в стенке сосуда, и в окружающих сосуд тканевых элементах. Понятно также, что этот процесс приводит к существенным нарушениям просвета сосудов — сужению и облитерации их.
Плазматическое пропитывание артериол, приводящее к артериолонекрозу, несомненно представляет собой тяжелейшее проявление болезни вторичного характера. Вопрос о том, чем именно оно обусловлено, пока достаточно не выяснен. Конечно, играет роль повышение внутриартериального давления, поскольку этот фактор должен облегчать и усиливать механическую импрегнацию сосудов белковыми массами.
Возникает вопрос, нет ли каких-либо других факторов, которые были бы ответственны за развитие плазморрагий и артериолонекроза при гипертонии. Выдвигается предположение о трофических изменениях мелких сосудов при гипертонии. Согласно этому предположению, расстройство проницаемости мелких сосудов и связанная с ними белковая инфильтрация сосудистых стенок не являются простым следствием повышения внутриартериального давления, а есть скорее результат нарушения питания самих стенок сосудов. Последние могут зависеть от разных причин:
- во-первых, само сокращение мышечной оболочки сосудов может ухудшать условия снабжения стенок артерий питательными материалами;
- во-вторых, питание сосудистых стенок может страдать вследствие свойственного больным гипертонией сужения артериального русла;
- в-третьих, можно предположить и нейрогенные влияния на трофику сосудистых стенок, возникающие при нарушении тех условий адаптации сосуда как эфферентного органа к функциональной нагрузке, которые осуществляются нервными импульсами, идущими с центра.
С этой последней точки зрения изменения сосудов при гипертонии развиваются не столько вторично относительно гипертонии, сколько параллельно ей; они обусловлены одним и тем же первичным нарушением регулирующей роли нервной системы.
Липоидная инфильтрация мелких стенок артерий лишь в слабой степени выражена при белковой инфильтрации. Зато в крупных артериях эластического типа липоидоз (атеросклероз) наблюдается весьма часто и достигает большой степени. Частое развитие при гипертонической болезни атеросклероза подтверждается большинством врачей. Необходимо отметить, что механизм развития липоидоза сосудов при гипертонии, по-видимому, весьма близок к тому, который определяет и белковое пропитывание.
Помимо наклонности к атеросклерозу, наблюдается преждевременное «старение» сосудов при гипертонии в связи с превращением эластических (свежих) волокон в старые фиброзные (эластофиброз). Возможно, что это явление — результат механического перерастяжения и рабочей перегрузки сосудов под влиянием гипертензии, но нельзя исключить значение отмеченных выше нарушений трофики этих сосудов.
Необходимо указать на изменения vasa vasorum крупных сосудов при гипертонии. Они проявляются гиалинозом и артериолонекрозом. Вероятно, этими изменениями объясняются редкие случаи разрыва крупных сосудов, в том числе аорты, при гипертонии. Что тут играет роль не только атеросклероз аорты, видно из случаев разрыва аорты без атеросклеротических изменений, иногда в сравнительно молодом возрасте. Эти разрывы происходят обычно вблизи от аортальных клапанов. Данная локализация разрывов понятна с гемодинамической точки зрения — она обусловлена тем резким напряжением, которое претерпевает аорта в этом месте под давлением ударного объема крови, выбрасываемой левым желудочком и встречающей препятствия в виде аортальной дуги. Но известны и другие локализации разрывов сосудов при гипертонии. Иногда возникает только разрыв внутренней артериальной оболочки с последующим образованием aneurysma dissecans.
Разрывы более мелких сосудов могут объяснить возникновение при гипертонической болезни легочных, кишечных и других кровотечений, а также кровоизлияний в тех или иных органах; иногда речь идет о разрывах мелких аневризм, образующихся по ходу периферических артерий.
Для понимания морфологических изменений сосудов при гипертонии представляются весьма демонстративными данные, которые были получены при гипертонических кризах. Все изменения сосудов при гипертонических кризах делят условно на три степени.
- Первая степень — начальные, скоропреходящие изменения в виде пропитывания белками плазмы субэндотелиального слоя.
- Вторая степень — более глубокое проникновение белковых масс в толщу сосудистой стенки, пропитывание последней ими, что приводит к очагам некробиоза, пристеночному тромбозу, развитию милиарных аневризм и периваскулярных кровоизлияний.
- Третья степень — разрывы и некроз сосудистой стенки с кровоизлиянием в окружающие ткани.
Возможно, что эти степени отражают в одних случаях нарастающую картину криза, и тогда они могут быть обозначены стадиями его; но не исключено, что они отражают интенсивность, тяжесть криза. Во всяком случае картины, описанные при кризах, могут быть проецированы и на разные этапы или степени сосудистых изменений при гипертонической болезни вообще, поскольку криз является не чем иным, как «сгустком» болезни, в котором отражена ее эволюция (но в быстрой, концентрированной форме).
Изменения сосудов при гипертонии зависят от:
- степени нагрузки на сосуды, обусловленной повышением кровяного давления,
- степени участия тонических изменений сосудистой стенки в различных органах.
Оба эти фактора, конечно, могут сочетаться. В последнее время привлекают внимание так называемые фибриноидные некрозы сосудистых стенок при эссенциальной гипертонии. Их считают наиболее частой формой поражения сосудов при этой болезни. Особенно часто находят их при так называемой злокачественной гипертонии, при гипертонических изменениях в почках, а также в опытах с воспроизведением почечной гипертонии. Артериолонекроз (фибриноидный) некоторые авторы даже склонны считать воспалительным процессом — артериолитом.
Возникли вопросы или что-то непонятно? Спросите у редактора статьи —
здесь
.
Различают альтеративный артериолит, как он наблюдается, например, при узелковом периартериите и других аллергических заболеваниях (при этом сначала повреждается артериальная стенка, а затем она пропитывается фибрином), и экссудативный артериолит (при этом фибрин проникает в неизмененную сосудистую стенку), как при эссенциальной гипертонии. Фибриноидный некроз при гипертонии давал повод рассматривать изменения в сосудах как проявление аллергии или относить их в группу патологических процессов, объединяемых понятием коллагеноза. Но прав Goldblatt, который отрицает такую точку зрения на сосуды при гипертонии, считая, что изменения описанного типа только напоминают узелковый периартериит. Фибриноидные очаги в стенках артерий представляют собой лишь проявление реакции в ответ на некрозы, образующиеся там, а не носят первичного характера. Фибриноидный некроз при гипертонической болезни не есть какой-то особый некроз, а некроз, развивающийся в соединительной ткани; он вторичный, следующий за плазморрагией.
Статью подготовил и отредактировал: врач-хирург Пигович И.Б.
Видео:
Полезно:
Источник
… наиболее характерным признаком гипертонической болезни является изменения артериол.
Суть ремоделирования заключается в способности органа изменять структуру и геометрию в ответ на долговременное воздействие патологических стимулов. Ремоделирование с точки зрения патофизиологии означает обретение новой функции биологической структурой. Рассмотрим процесс ремоделирования сосудов в рамках артериальной гипертензии.
Ремоделирование сосудов – это неизменный атрибут артериальной гипертензии, проявляющийся адаптивной модификацией функции и морфологии сосудов, которая (адаптивной модификацией) является с одной стороны, осложнением, с другой – фактором прогрессирования артериальной гипертензии.
Процесс ремоделирования сосудов при артериальной гипертензии включает две стадии: (1) стадию функциональных изменений сосудов, связанную с вазоконстрикторными реакциями в ответ на трасмуральное давление и нейрогуморальную стимуляцию, и (2) морфологическую стадию, характеризующуюся структурным уменьшением просвета сосудов вследствие утолщения их медиального слоя.
Стадия функциональных изменений сосудов в виде вазоконстрикторной реакции в «континууме ремоделирования сосудов» при артериальной гипертензии начинается обычно как адаптивный процесс в ответ на изменение условий гемодинамики или активности тканевых и циркулирующих гуморальных факторов. Длительно существующая адаптация сменяется нарушением структуры сосудов в ответ на изменение гемодинамической нагрузки, а также в ответ на повреждение токсичными веществами, метаболитами и атерогенными факторами. В последующем структурные повреждения сосудов проявляются нарушениями их функций (проводящей и/или демпфирующей), что последовательно ведет к расстройству кровообращения органов и нарушению их функций.
Прежде чем рассматривать «структурное» (морфологическое) ремоделирование сосудов при артериальной гипертензии необходимо рассмотреть строение основной ее «мишени» (точки приложения), то есть строение артериальной стенки.
Артериальная стенка состоит из соединительнотканных структур, разделяющихся на три слоя:
(1) внутренняя оболочка (tunica intima, интима) – является барьером между артериальной стенкой и кровью, состоит из одного слоя эндотелиальных клеток, тонкого субэндотелиального слоя и базальной мембраны;
(2) средняя оболочка (tunica media, медиа) — это наиболее широкий слой артериальной стенки, который состоит из относительно большого количества гладкомышечных клеток и миофибробластов; сокращение и расслабление мышечных элементов меди изменяют просвет сосуда в ответ на действие различных системных и локальных вазоактивных соединений;
(3) внешняя оболочка (tunica adventitia, адвентиция) – состоит из соединительной ткани, содержащей волокна гладкомышечных клеток, фибробласты, мелкие артерии и вены, связанные с периадвентицией и жировой тканью, поддерживающей сосуд.
Следует отметить тот факт, что сосуды большого — аорта, проксимальный отдел аортальных коллатералей и легочная артерия калибра — являются сосудами эластического типа и не обладают функцией сократимости, но эффективно сдерживают давление тока крови. При артериальной гипертензии наиболее значимые патофизиологические изменения происходят в мелких сосудах.
Согласно закону Пуайзеля, детерминантами артериального сопротивления являются вязкость крови, длина и калибр сосуда. Но так как длина сосуда и вязкость крови являются относительно постоянными величинами, размер сосуда может изменяться в результате резких изменений тонуса или вследствие длительного процесса ремоделирования. Свойства стенки сосуда зависят от двух характеристик: (1) растяжимости (прямо пропорциональной давлению и радиусу и обратно пропорциональной толщине стенки) и (2) напряжению сдвига (комплекс сил, действующих на сосудистую стенку в результате тока крови). Изменения радиуса и толщины стенки поддерживают эти две величины в относительно постоянном состоянии. При повышенном токе крови радиус сосуда увеличивается для снижения напряжения сосудистой стенки. При высоком внутрисосудистом давлении компенсаторно увеличивается толщина сосуда и уменьшается диаметр.
Помимо баланса биомеханических сил на структурные (морфологические) элементы артериальной стенки оказывают влияние целый ряд биологически активных веществ, в частности катехоламины, ангиотензин II, эндотелин-1, сосудисто-эндотелиальный фактор роста и некоторые другие факторы.
Катехоламины, обладая трофической функцией, стимулируют гипертрофию гладкомышечных клеток сосудов. Трофический эффект адренергической стимуляции реализуется прямо или опосредованно через увеличение секреции тромбоцитарного ростового фактора. Способность ангиотензина II стимулировать гипертрофию и гиперплазию гладкомышечных клеток сосудов продемонстрированa в культуральных условиях и на примере экспериментальных животных. Кроме того, ангиотензин II может выступать в роли паракринного регулятора продукции ряда пептидных ростовых факторов клетками сосудистой стенки и клетками крови. К таким факторам, уровень которых повышается под влиянием ангиотензина II, относятся тромбоцитарный ростовой фактор и 1-трансформирующий фактор. Последние участвуют в модификации гипертрофического эффекта ангиотензина II на гладкомышечные клетки сосудов.
Различают (1) концентрическое ремоделирование, при котором уменьшается просвет сосуда, и (2) эксцентрическое, при котором просвет увеличивается. Концентрическое сосудистое ремоделирование обычно развивается при повышенном внутрисосудистом давлении или снижении тока крови, в то время как эксцентрическое ремоделирование развивается при повышении тока крови.
Гистологическими характеристиками эксцентрического ремоделирования являются: истончение стенки сосуда, снижение гладкомышечного компонента медиа, уменьшение экстрацеллюлярного матрикса и снижение отношения толщины стенки сосуда и внутреннего диаметра. При этом варианте ремоделирования сосудов выявляют дегенеративные изменения медиа с повышением в ней уровня коллагена, фиброэластическое утолщение интимы, фрагментацию эластической мембраны с вторичным фиброзом и кальцинозом медиа и изменения экстрацеллюлярного матрикса.
В отношении сосудистой массы выделяют эутрофический, гипертрофический и гипотрофический типы ремоделирования в зависимости от снижения, отсутствия изменений или увеличения клеточных компонентов (у больных с артериальной гипертензией чаще выявляются структурные изменения сосуда, преимущественно по гипертрофическому типу):
(1) эутрофическое внутреннее ремоделирование характеризуется уменьшением наружного диаметра и просвета сосуда, с отсутствием изменений толщины медиального слоя; этот вариант ремоделирования характеризуется увеличением отношения толщины медиального слоя к просвету сосуда без повышения жесткости сосудистой стенки и описан в резистивных артериях при мягком течении гипертонической болезни;
(2) эутрофическое наружное ремоделирование характеризуется увеличением просвета резистивных артерий без изменения площади поперечного сечения сосуда, что наблюдается при гипотензивной терапии у больных с эссенциальной гипертензией;
(3) гипертрофическое внутреннее ремоделирование характеризуется увеличением отношения медиа/просвет сосуда за счет утолщения медиального слоя; этот тип ремоделирования выявлен у больных с симптоматическими гипертензиями (а также при экспериментальной дезоксикортикстероновой солевой гипертензии, реноваскулярной гипертензии на модели «одна почка – один зажим»);
(4) гипотрофическое наружное ремоделирование характеризуется увеличением просвета сосуда с уменьшением площади его поперечного сечения (данный вид ремоделирования выявлен у спонтанногипертензивных крыс на фоне гипотензивной терапии).
На сегодняшний день установлено что:
(1) у больных гипертонической болезнью, как правило, закономерным является гипертрофия артериальных сосудов, которая выражается в дилатации артерий эластического типа и утолщении стенки артерий эластического и мышечного типа, причем по мере увеличения степени тяжести артериальной гипертензии наблюдается прогрессирование артериальной гипертрофии.
(2) на гипертрофию артериальной стенки может влиять целый ряд факторов, среди которых основная роль принадлежит локальным гемодинамическим условиям, в частности балансу биомеханических сил, оказывающих влияние на артериальную стенку, а также гуморальным факторам, стимулирующим процессы клеточного роста и гипертрофии.
Источник

