Порочный круг при гипертонии
1. Гипотеза Э. Гелльгорна и соавт.
Инициальным патогенетическим фактором является стойкая повышенная возбудимость и реактивность (гиперергия) высших симпатических нервных центров (в частности, расположенных в заднем отделе гипоталамуса). Факторами, вызывающими стойкую гипе-рергию этих центров, является длительное, повторное возбуждение эмоциональных центров, тесно связанных с симпатическими ядрами гипоталамуса.
Повышение тонуса прессорных (симпатических) центров ведет к спазму сосудов, увеличению сердечного выброса и повышению АД, обусловливает гиперпродукцию гуморальных факторов с прессорным действием адреналина, норадреналина, вазопрессина,
АКТГ, кортикостероидов, а также гиперсекрецию ренина в юкстагломерулярном аппарате (ЮГА) почек.
2, Гипотеза Е. Муирад, А. Гайтона и соавт.
Инициальным фактором развития гипертензии является генетически обусловленный пониженный уровень ЫаС1- и водовыделительной функции почек, что ведет к накоплению избытка натрия и воды в организме, включая ткань сосудистых стенок, в том числе их гладкие мыпщы. В связи с этим развивается гиперволемия, повышаются тонус сосудов и чувствительность их стенок к прессорным гормонам и другим биологически активным факторам.
3, Гипотеза нарушения функций мембранных ионных насосов проф. Ю.В. Постнова.
Инициальным фактором в патогенезе артериальной гипертензии является генерализованный наследственный дефект мембранных ионных насосов клеток, включая глад» комышечные клетки стенок артериол. Дефект этот заключается в снижении активности кальциевого насоса, локализующегося в мембранах эндоплазматической сети, и натриевого насоса, локализующегося в плазмолемме. В результате уменьшается «откачивание» Са+2 из цитоплазмы в эндоплазматическую сесть и Иа+ из цитоплазмы в межклеточное пространство. Избыток Са+2 и Ыа+ в цитоплазме гладкомышечных клеток сосудов вызывает их спазм, а также повышение чувствительности к прессорным факторам.
4, Гипотеза проф. Г Ф. Лонга и проф. А.Л. Мясникова.
Инициальным патогенетическим фактором развития ГБ является растормажива-ние центров ССС (снижение тормозного влияния коры головного мозга на подкорковые вегетативные нервные центры, прежде всего пресеорные).
Этиологическими факторами являются стрессоры. Первичное звено патогенеза -возбуждение симпатических центров -> включение еимпатоадреналовой реакции, подключение ЮГА почек -» альдостерон -» накопление Иа»1″ -» увеличение ОЦК + набухание сосудистой стенки .*-» повышение ее реактивности. Длительный спазм гладких мышц сосудов -> накопление Са+2 в цитоплазме мышечных волокон -» активация РНК-полимеразы -> гипертрофия гладкомышечных элементов сосудистой стенки.
Клинико-потегенетинеские формы эссенциальной гипертонии[по Кушаковско-му].
1. Гиперадренерическая (Ланг, Мясников).
2. Гипергидратационная.
3. Ангиотензин-зависимая.
4. Кальций-зависимая (Постнов, Орлов).
5. Цереброишемичеекая.
В табл. 3.7.3. и 3.7.4. представлены прогностические факторы артериальной гипертензии (стратификация факторов риска).
Стратификация риска ГБ позволяет врачу составить более объективное (хотя и упрощенное) представление о долговременном прогнозе заболевания у каждого конкретного больного с целью выбора оптимальной тактики индивидуального лечения.
А. Факторы риска сердечнососудистых заболеваний
В. Поражение органов-мишеней
С. Сопутствующие клинические состояния
I. Используемые для оценки риска
Уровни систолического и диастоличе-ского АД (артериальная гипертензия 1-3 степени)
Мужчины старше 55 лет
Женщины старше 65 лет
Курение
Уровень сыворотки общего холестерина более 6,5 ммоль/л (250 мг/дл)
Сахарный диабет
Указания на преждевременное развитие сердечно-сосудистого заболевания в семейном анамнезе
И. Другие факторы, оказывающие неблагоприятное влияние на прогноз
Пониженные уровни холестерина ЛПВП
Повышенные уровни холестерина ЛПНП
Микроальбуминурия (30-300 мг/сут) при сахарном диабете
Нарушенная толерантность к глюкозе
Ожирение
Сидячий образ жизни
Повышенные уровни фибриногена
Социально-экономическая группа с высоким риском
Этническая группа с высоким риском
Географический регион с высоким риском
Гипертрофия левого желудочка (по данным электрокардиографии, эхокардио-графии или рентгенографии органов грудной клетки)
Протеинурия (>300 мг/сут) и/или небольшое повышение концентрации креати-нина в плазме (1,2-2,0 мг/дл)
Ультразвуковые или рентге-ноангиографнческие признаки атеросклеротического поражения сонных, подвздошных и бедренных артерий, аорты
Генерализованное или фокальное еужение артерий сетчатки
Сосудистое заболевание головного мозга
Ишемический инсульт
Геморрагический инсульт
Преходящее нарушение мозгового кровообращения
Заболевание сердца
Инфаркт миокарда
Стенокардия
Реваскуляризация коронарных артерий
Застойная сердечная недостаточность
Заболевание почек
Диабетическая нефропатия
Почечная недостаточность (содержание креатинина в плазме крови выше 2,0 мг/дл)
Сосудистое заболевание
Расслаивающая аневризма
Поражение артерий с клиническими проявлениями
Выраженная гипертоническая ретинопатия
Кровоизлияния или экссудаты
Отек соска зрительного нерва
Примечание. Поражения органов-мишеней (ПОМ) соответствуют II стадии гипертонической болезни по классификации экспертов ВОЗ 1996 г., а сопутствующие клинические состояния — III стадии заболевания.
| Таблица 3.7.4. Уровень риска сердечно-сосудистых осложнений у больных с артериальной гипертензией разной степени с целью определения прогноза* [по ВОЗ-МОГ, 1999]. | |||
| Факторы риска (кроме артериальной гипертензии) и анамнез болезни | Уровень риска при артериальной гипертензии | ||
| 1-я степень («мягкая») | 2-я степень («умеренная») | 3-я степень («тяжелая») | |
| : Нет других факторов риска | Низкий | Средний | Высокий |
| 1-2 других фактора риска | Средний | Средний | Очень высокий |
| 3 и более других факторов риска, ПОМ или сахарный диабет | Высокий | Высокий | Очень высокий |
| Сопутствующее заболевание* * | Очень высокий | Очень высокий | Очень высокий |
* Типичные примеры риска развития мозгового инсульта или инфаркта за 10 лет: низкий риск — менее 15%; средний риск — примерно 15-20%; высокий риск — примерно 20-30%; очень высокий риск — 30% или выше. ** См. табл. 3.7.3. ПОМ — поражение органов-мишеней (см. табл. 3/7.3Л.
Порочные круги при гипертонической болезни:
1. Рениновый: повышение АД ~» артериальный спазм -> ишемия почек -* выброс ренина из ЮГА -> активация РААС -> повышение АД.
2. Сердечный: гиперволемия ~» закон Анрепа (сила сердечных сокращений пропорциональна давлению (сопротивлению), против которого она работает) г-» рост УО ~» повышение АД.
3. Атеросклероз вызывает поражение депрессорных зон.
4. Сосудистый: спазм гладких мышц сосудов -» накопление Са+2 в цитоплазме мышечных волокон -> активация РНК-полимеразы -» гипертрофия и гиперплазия гладкомы-шечных элементов сосудистой стенки.-» повышение периферического сосудистого сопротивления.
///. Симптоматические гипертензии.
Симптоматические (вторичные) артериальные гипертонии (гипертензии)—
стойкое повышение АД, являющееся проявлением (симптомом) какого-либо заболевания.
1. Почечные артериальные гипертензии:
■ Вжоренолъная: атеросклероз почечной артерии, фибромускулярная дисплазия, аор-тоартериит, васкулиты, эндартериит, тромбоз, эмболия, аневризмы почечной артерии, атрезия и гипоплазия почечных артерий, артериовенозные фистулы, стенозы и тромбозы вен, гематомы, травмы сосудов почек; неоплазмы, сдавливающие почечные артерии -> ишемия почек -» выброс ренина из ЮГА -» активация РААС -> повышение АД.
■ Реноприеная: поражение (гломерулонефрит, хронический пиелонефрит, диабетический гломерулосклероз, амилоидоз, гидронефроз) или удаление паренхимы почек -> дефицит почечных простагландинов А и Е -> повышение АД.
2. Эндокринные артериальные гипертензии:
■Минералокортикоидные (первичный альдостеронизм или синдром Конна): гипер
плазия или опухоль клубочковой зоны коры надпочечников -> повышение продук
ции альдостерона -» усиление реабсорбции Ка+ и воды -» увеличение концентра
ции Ка+ в плазме -» гиперосмия плазмы -» стимуляция секреции вазопрессина ->
рост ОЦК -> повышение АД.
Увеличение концентрации Ка* в плазме -» повышение транспорта ионов Иа* через мембраны клеток -» накопление избытка Ка+ в клетках -» набухание клеток, в том
числе и стенок сосудов -» сужение их просвета + увеличение чувствительности к катехоламинам, вазопресеину, АГИ-» повьппение АД.
■ Глюкокортикоидные: гиперплазия или гормонально-активные опухоли пучковой зоны коры надпочечников (синдром Иценко-Кушинга) и базофильных клеток передней доли гипофиза (болезнь Иценко-Кушинга) .-> пермиссивное действие глю-кокортикоидов на эффект адреналина + слабая минералокортикоидная активность глюкокортикоидов -» повьппение АД.
■ Катехоламиновые: феохромоцитома (опухоль мозгового вещества надпочечников) -» гиперпродукция адреналина и норадреналина -> повышение АД.
■ Гипертиреоидные: тиреотоксикоз -» гиперпродукция тироксина и трийодтиронина -» увеличение силы и частоты сердечных сокращений (прямое кардиостимули-рующее действие гормонов + увеличение чувствительности сердца к катехолами-нам)^ увеличение УО -> повышение АД.
■ Вазопрессиновые: повышение секреции гипоталамусом вазопрессина (вазопресси-нома) -» сужение сосудов + задержка воды с увеличением ОЦК -» повышение АД.
3. Нейрогенные артериальные гипертензииформируются при органических поражениях нервных структур (сосудистые, воспалительные заболевания, опухоли ЦНС, травмы мозга), регулирующих системную гемодинамику (нервы, продолговатый, спинной мозг, гипоталамус, кора больших полушарий) -» преобладание прессорных влияний над депрес-сорными.
4. Гемодинамические артериальные гипертензиивозникают при поражении сердца и крупных сосудов:
■ Атеросклероз аорты -> поражение делрессорных зон аорты -> повьппение АД.
■ Коарктация аорты -> по закону Анрепа (сила сердечных сокращений пропорциональна давлению (сопротивлению), против которого она работает) -> рост УО -» повышение АД.
■ Недостаточность аортальных клапанов -> рост УО по закону Франка-Старлинга (чем больше наполняется сердце во время диастолы, тем сильнее оно сокращается в систолу) -» повьппение АД.
■ Полная атриовентрикулярная блокада.
■ Реологическая гипертензия: увеличение вязкости крови (болезнь Вакеза, полици-темия, эритроцитозы, гиперпротеинэмия) -> повышение АД.
■ Васкулиты (аорто-артериит или болезнь Такаясу) -> уменьшение диаметра сосудов -> повышение АД.
Источник
Гипертоническая
болезнь –
артериальная гипертензия неизвестной
этиологии. Диагноз гипертонической
болезни (эссенциальной, первичной АГ)
устанавливают методом исключения
вторичных (симптоматических) артериальных
гипертензий.
Определение
«эссенциальная» означает, что стойко
повышенное АД при гипертонической
болезни составляет сущность этой
артериальной гипертензии. Каких-либо
изменений в других органах, которые
могли бы привести к артериальной
гипертензии, при обычном обследовании
не находят.
Классические
концепции этиологии и патогенеза
эссенциальной АГ включают нейрогенную
теорию Г.Ф.Ланга-А.Л.Мясникова, мембранную
Ю.В.Постнова-С.Н.Орлова, объемно-солевую
А.Гайтона, церебро-ишемическую Диккинсона.
Нейрогенная
теория Г.Ф.Ланга – А.Л.Мясникова.
Согласно концепции, разработанной Г.Ф.
Лангом и А.Л. Мясниковым, «нервное
перенапряжение при гипертонической
болезни реализуется в расстройстве
трофики определенных мозговых структур,
управляющих АД. Об этом свидетельствуют
частые случаи развития первичной
гипертензии у людей «стрессовых»
профессий. Особое значение при этом
имеют отрицательные эмоции, в частности
эмоции, не
отреагированные в двигательном акте,
когда вся сила их патогенного воздействия
обрушивается на систему кровообращения.
На этом основании Г.Ф. Ланг назвал
гипертоническую болезнь «болезнью
неотреагированных эмоций».
Непосредственный
механизм повышения АД связан с
возникновением очага
застойного возбуждения (патологической
доминанты, по терминологии А.А. Ухтомского)
вегетативных центров головного мозга,
в первую очередь сосудодвигательного
центра.
Стресс вызывает
активацию гипофизарно-надпочечниковой
и симпатоадреналовой системы с последующим
включением прессорного механизма РААС.
Это приводит к увеличению сердечного
выброса (МОК) при неизменной или слегка
сниженной величине ОПСС.
Рассмотренные
процессы формируются на первой
стадии гипертонической болезни,
которая называется транзиторной
(преходящей) и клинически характеризуется
непродолжительными эпизодами повышения
АД.
На второй стадии
гипертонической болезни (стадия
стабильной АГ) увеличение АД и местного
кровотока приводит к увеличению
сосудистого тонуса и генерализованному
спазму артериол (повышению ОПСС),
направленному на приведение в соответствие
местного кровотока и потребности в нем
тканей.
В происхождении
стабильного повышения тонуса сосудов
имеют значение формирующиеся в этой
стадии «порочные
круги» (рис.
1): барорецепторный, почечный (с участием
ЮГА), гипофизарно-надпочечниковый и
сосудистый (повышение чувствительности
стенки сосудов к катехоламинам).
В результате
повышения АД развивается парабиоз
барорецепторов сосудов и выпадает их
тормозной контроль над нейронами
сосудодвигательного центра. В итоге
тонус сосудов повышается еще сильнее.
Спазм сосудов
приводит к гипоксии ЮГА почек и активации
РААС.
В свою очередь,
ишемическая стимуляция аденогипофиза
реализуется в секреции АКТГ и,
следовательно, повышении содержания в
крови гормонов коры надпочечников
(минерало- и глюкокортикоидов). Поэтому
высокий тонус сосудов поддерживается
продолжительное время.
В механизме
гипертонии также играет роль повышение
чувствительности стенки сосудов к
катехоламинам, и даже небольшие дозы
адреналина оказывают выраженный
вазоконстрикторный эффект.
Таким образом,
определяющую роль в патогенезе АГ играют
изменения нейрогуморальной регуляции
сосудистого тонуса.
Конечным звеном
этого патологического процесса является
изменение функциональной активности
ионотранспортирующих систем плазматической
мембраны, что ведет к перегрузке
гладкомышечных клеток ионами Cа2+
и патологическому повышению тонуса
кровеносных сосудов. Такая концепция
патогенеза артериальной гипертензии
была выдвинута Ю.В.
Постновым и С.Н. Орловым,
которые назвали ее мембранной
концепцией.
Объемно-солевая
теория А. Гайтона.
Согласно этой теории, в основе развития
эссенциальной АГ лежит ослабление
выделительной функции почек, которое
приводит к задержке в организме ионов
Na+ и воды, а, следовательно, к увеличению
ОЦК и МОК.
При этом повышение
АД играет компенсаторную роль –
необходимо для обеспечения адекватного
натрийуреза и диуреза.
В ответ на повышение
МОК, местные механизмы саморегуляции
кровотока вызывают миогенное сужение
артериол, результатом которого является
нормализация МОК за счет повышения ОПСС
и тем самым повышения АД. Увеличению
выраженности и стойкости этой
констрикторной реакции способствует
повышение реактивности сосудов вследствие
отека и аккумуляции ионов Na+ в их стенке.
Таким образом, с
течением времени «гипертензия
выброса» со
свойственным ей гиперкинетическим
типом изменений гемодинамики (увеличение
МОК при нормальном ОПСС) трансформируется
в «гипертензию
сопротивления»
с гипокинетическим гемодинамическим
профилем (увеличение ОПСС при нормальном
или сниженном МОК).
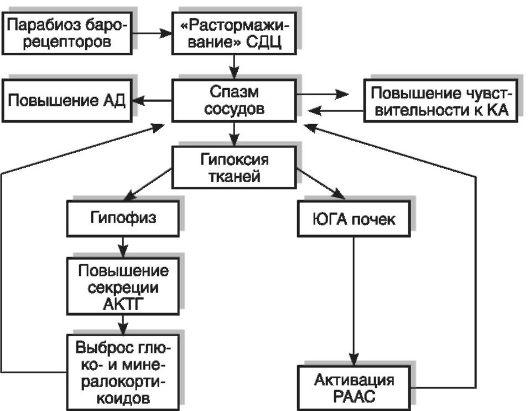
Рис. 1. «Порочные
круги» в
патогенезе гипертонической болезни:
АД — артериальное давление; АКТГ —
адренокортикотропный гормон; КА —
катехоламины; СДЦ — сосудодвигательный
центр; РААС — ренинангиотензин-альдостероновая
система; ЮГА — юкстагломерулярный
аппарат.
Церебро-ишемическая
теория Диккинсона. Уменьшение
объемной скорости кровотока в сосудах
головного мозга (атеросклероз, спазм
церебральных сосудов и т.д.) вызывает
ишемию мозга. Реакция на ишемию головного
мозга начинается с хеморецепторов,
расположенных в ЦНС, что приводит к
активации прессорного отдела
сосудодвигательного центра, сильной
симпатической вазоконстрикции,
стимуляции сердечной деятельности.
Увеличение системного АД позволяет в
определенной степени улучшить
кровоснабжение мозга, однако поддержание
стабильно высокого АД не может
осуществляться только за счет спазма
сосудов. Ишемия ЦНС, по-видимому, является
только инициирующим звеном АГ.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Рениновый: АД артериальный спазм ишемия почек выброс ренина из ЮГА активация РААС АД.
Сердечный: гиперволемия закон Анрепа (сила сердечных сокращений пропорциональна давлению (сопротивлению), против которого она работает) рост УО АД.
Атеросклероз поражение депрессорных зон.
Сосудистый: спазм гладких мышц сосудов накопление Ca +2 в цитоплазме мышечных волокон активация РНК-полимеразы гипертрофия и гиперплазия гладкомышечных элементов сосудистой стенки. периферического сосудистого сопротивления.
Гипертонический криз — одно из наиболее частых и тяжелых осложнений гипертонической болезни и симптоматических артериальных гипертензий, характеризующееся острым повышением артериального давления до индивидуально высоких цифр и резким обострением симптоматики заболевания с преимущественным преобладанием церебральных и сердечно сосудистых расстройств.
Вторичная (некардиогенная) сердечная недостаточность, гипертрофия миокарда, инфаркт миокарда.
Инсульт (ишемический и геморрагический).
Первично-сморщенная почка (артериологиалиноз и артериолосклероз почечных сосудов нарушение почечной гемодинамики структурные изменения в нефронах и интерстициальной ткани постепенно нарастающая гибель почечных нефронов, сопровождающаяся уменьшением массы действующих нефронов), клиническим проявлением которой является хроническая почечная недостаточность (никтурия, полиурия, понижение относительной плотности мочи, азотемия).
67. – Особенности этиологии и патогенеза различных видов симптоматических артериальных гипергензий.
Симптоматические гипертензии. Патогенетическая классификация. Осложнения артериальных гипертензий.
Симптоматические (вторичные) артериальные гипертонии (гипертензии) — стойкое повышение АД, являющееся проявлением (симптомом) какого-либо заболевания.
Почечные артериальные гипертензии
Вазоренальная: атеросклероз почечной артерии, фибромускулярная дисплазия, аортоартериит, васкулиты, эндартериит, тромбоз, эмболия, аневризмы почечной артерии, атрезия и гипоплазия почечных артерий, артериовенозные фистулы, стенозы и тромбозы вен, гематомы, травмы сосудов почек; неоплазмы, сдавливающие почечные артерии ишемия почек выброс ренина из ЮГА активация РААС АД.
Ренопривная: поражение (гломерулонефрит, хронический пиелонефрит, диабетический гломерулосклероз, амилоидоз, гидронефроз) или удаление паренхимы почек дефицит почечных простагландинов А и Е) АД.
Эндокринные артериальные гипертензии
Минералокортикоидные (первичный альдостеронизм или синдром Конна): гиперплазия или опухоль клубочковой зоны коры надпочечников повышение продукции альдостерона усиление реабсорбции Na + и воды увеличение концентрации Na + в плазме гиперосмия плазмы стимуляция секреции вазопрессина рост ОЦК АД.
увеличение концентрации Na + в плазме повышение транспорта ионов Na + через мембраны клеток накопление избытка Na + в клетках набухание клеток, в том числе и стенок сосудов сужение их просвета + увеличение чувствительности к катехоламинам, вазопрессину, АГII АД.
Глюкокортикоидные: гиперплазия или гормонально-активные опухоли пучковой зоны коры надпочечников (синдром Иценко-Кушинга) и базофильных клеток передней доли гипофиза (болезнь Иценко-Кушинга) пермиссивное действие глюкокортикоидов на эффект адреналина + слабая минералокортикоидная активность глюкокортикоидов АД.
Катехоламиновые: феохромоцитома (опухоль мозгового вещества надпочечников) гиперпродукция адреналина и норадреналина АД.
Гипертиреоидные: тиреотоксикоз гипертиреоидный зоб щитовидной железы и т.п. гиперпродукция тироксина и трийодтиронина увеличение силы и частоты сердечных сокращений увеличение УО АД.
гиперпродукция тироксина и трийодтиронина увеличение чувствительности сердца к катехоламинам АД.
Вазопрессиновые: повышение секреции гипоталамусом вазопрессина (вазопрессинома) сужение сосудов + задержка воды с увеличением ОЦК АД.
Нейрогенные артериальные гипертензии (при заболеваниях и поражениях нервной системы)
Органические поражения (сосудистые заболевания и опухоли мозга, воспалительные заболевания ЦНС (энцефалит, менингит, полиомиелит, диэнцефальный синдром), травмы мозга (посткоммоционный и постконтузионный синдром), полиневриты) нервных структур, регулирующих системную гемодинамику (нервы, продолговатый, спинной мозг, гипоталамус, кора больших полушарий) преобладание прессорных влияний над депрессорными.
Гемодинамические артериальные гипертензии (при поражении сердца и крупных сосудов)
Атеросклероз аорты поражение депрессорных зон аорты АД.
Стенозирующее поражение сонных и вертебробазилярных артерий
Коарктация аорты по закону Анрепа (сила сердечных сокращений пропорциональна давлению (сопротивлению), против которого она работает) рост УО АД.
Недостаточность аортальных клапанов рост УО по закону Франка-Старлинга (чем больше наполняется сердце во время диастолы, тем сильнее оно сокращается в систолу, т.е. ударный объем возрастает по мере увеличения наполнения сердца) АД.
Полная атриовентрикулярная блокада.
Реологическая гипертензия: увеличение вязкости крови (болезнь Вакеза, полицитэмия, эритроцитозы, гиперпротеинэмия) АД.
Васкулиты (аорто-артериит или болезнь Такаясу, васкулиты сосудов среднего и мелкого диаметра) уменьшение диаметра сосудов АД.
Особые формы вторичных артериальных гипертензий
Солевая и пищевая гипертензия (при чрезмерном употреблении соли, при употреблении веществ, богатых тирамином — некоторые сорта сыра и марки красного вина).
Медикаментозные гипертензии (при приеме глюкокортикоидов и минералокортикоидов, контрацептивных препаратов, содержащих прогестерон и эстроген, инфекундина, производных глицирризиновой кислоты (карбеноксолон), симпатических аминов, лакричного порошка, индометацина и др.).
68. – Артериальные гипотонии. Виды. Этиология. Патогенез.
Артериальная гипотония характеризуется снижением артериального давления ниже 100/60 мм рт.ст. (для лиц в возрасте до 25 лет) и ниже 105/65 мм рт.ст. (для лиц старше 30 лет).
Гипотензия артериальная ортостатическая — снижение артериального давления систолического в ортостатическом положении на 20 мм рт.ст. и более.
Физиологическая артериальная гипотония, обусловленная в основном конституциональными и наследственными факторами, встречается нередко у совершенно здоровых людей, выполняющих обычную физическую работу, и не сопровождается какими-либо жалобами и патологическими изменениями в организме. Известна физиологическая гипотония проходящего характера у спортсменов.
Патологическая артериальная гипотония
1. Гипотоническая болезнь (первичная артериальная гипотония, нейроциркуляторная дистония по гипотоническому типу, нейроциркуляторная гипотония) — заболевание, характеризующееся стойким снижением АД.
В основе первичной артериальной гипотонии лежит повышение тонуса парасимпатического отдела вегетативной нервной системы, нарушение функции высших вегетативных центров вазомоторной регуляции, ведущее к стойкому уменьшению общего периферического сопротивления току крови. Компенсаторное увеличение сердечного выброса в этих случаях оказывается недостаточным для нормализации артериального давления. Скорость кровотока при первичной хронической артериальной гипотонии обычно не изменена. Объём циркулирующей крови находится в пределах нормы или несколько снижен, иногда имеется склонность к нормоволемической полицитемии.
Указанные сдвиги обусловлены, скорее всего, уменьшением глюкокортикоидной активности коры надпочечников при неизменной минералкортикоидной активности.
Основное значение в возникновении гипотонической болезни, по-видимому, принадлежит длительному психоэмоциональному напряжению, в отдельных случаях – психической травме. По современным представлениям, первичная гипотония является особой формой невроза высших сосудодвигательных центров с нарушением регуляции сосудистого тонуса.
2. Вторичная (симптоматическая) артериальная гипотония
Выделяют острые и хронические формы.
Причины хронической вторичной артериальной гипотензии:
Значительно выраженное варикозное расширение вен нижних конечностей.
Беременность поздних сроков.
Хроническая надпочечниковая недостаточность.
Длительный постельный режим.
Синдром гипербрадикинизма (отсутствуют киназы, расщепляющие брадикинин), наследственно обусловленный и приобретенный (при демпинг синдроме). Ортостатическая гипотензня при гипербрадикинизме возникает после еды, способствующей освобождению кининов из стенки кишечника и поджелудочной железы, и сопровождается ярким покраснением лица вследствие действия кининов на сосуды кожи.
Нарушение дуги барорефлекса на различных уровнях (при сухотке спинного мозга, B12-дефицитной анемии, хроническом алкоголизме, сахарном диабете, сирингомиелии, миелите, порфирии, полинейропатии Гийена-Барре).
Прием ганглиоблокаторов, изобарина, лабеталола, прозозина, нитратов.
69. – Патология сосудистого тонуса. Роль нервных, гуморальных, метаболических, миогенных факторов. Понятие дисфункций эндотелия и ее роль в механизмах нарушения сосудистого тонуса.
Сосудистая компонента – определяется сосудистым тонусом; существенно изменять свой диаметр способны только резистивные сосуды; интегральными показателями сосудистого тонуса являются общее периферическое сопротивление (ОПСС) и удельное периферическое сопротивление (УПСС).
Состояние тревоги возникает тогда, когда определенный раздражитель воспринимается как несущий в себе элементы опасности, угрозы, вреда. Переживание тревоги свойственно любому человеку в соответствующих ситуациях.
Цей документ складено відповідно до настанов Європейського товариства кардіологів (ESC), присвячених питанням терапії тромбоемболії легеневої артерії (ТЕЛА). Чинність багатьох положень цих настанов не втратила дійсності чи навіть отримала додаткове підтвердження, однак нові дані розширили й певним чином змінили наші знання, що стосуються оптимальної діагностики, оцінки та лікування пацієнтів із ТЕЛА.
В последнее время произошли существенные изменения в ведении пациентов с венозными тромбоэмболиями (ВТЭ). Как и прежде, антикоагулянтная терапия (АКТ) является основой лечения пациентов, однако на смену классическому варфарину пришли новые оральные антикоагулянты (НОАК), которые позволили повысить безопасность терапии, а также существенно упростили ее проведение в амбулаторных условиях. .
Острая декомпенсированная сердечная недостаточность (ОДСН) – это симптомокомплекс, возникающий при нарушении насосной функции сердца: снижении сердечного выброса (СВ), недостаточной перфузии тканей, повышенном давлении в легочных капиллярах, застое в тканях. Наиболее частой причиной (60-70%) ОДСН является ишемическая болезнь сердца (ИБС) [1, 2]. .
Во многих случаях изменения, первоначально возникшие в почках, играют ведущую роль в постепенном ухудшении ее функции и сопровождаются потерей нефронов, вынуждая по жизненным показаниям прибегать к лечению методом диализа или операции по пересадке почки. Это состояние называют терминальной стадией почечной недостаточности.
Исследования на лабораторных животных показали, что хирургическое удаление больших частей почек первоначально вызывает адаптивные изменения в оставшихся нефронах, которые приводят к усилению кровоснабжения почечной ткани, увеличению СКФ и сопровождаются увеличением выделения мочи у сохранившихся нефронов.
Точные механизмы, благодаря которым возникают указанные изменения, до конца не понятны. Они включают гипертрофию (рост различных структур у оставшихся нефронов), а также функциональные изменения, вследствие которых снижается сосудистое сопротивление и реабсорбция в канальцах.
Эти адаптивные изменения позволяют больным выделить нормальное количество воды и растворенных веществ, даже когда масса почечной ткани составляет 20-25% нормы. Тем не менее, в течение нескольких лет функциональные изменения почек способны привести к дальнейшему повреждению оставшихся нефронов, особенно в области клубочков.
Причина этого дополнительного повреждения не известна, однако некоторые исследователи полагают, что она может частично обусловливаться высоким давлением или перерастяжением стенок оставшихся клубочков, возникающих в результате функциональной вазодилатации или повышения артериального давления.
Постоянное увеличение давления, растяжение стенок небольших артериол и клубочков способно вызывать склерозирование этих сосудов (замену нормальной ткани соединительной). Развившиеся склеротические изменения в результате способны привести к облитерации просвета клубочка, способствуя дальнейшему ухудшению функции почек и новым адаптивным изменениям в оставшихся нефронах.
Эти изменения приводят к замыканию порочного круга, что неминуемо заканчивается терминальной стадией хронической почечной недостаточности. Единственным способом, объективно замедляющим потерю почками своих функций, служит снижение артериального и гидростатического давления в клубочках, особенно если с этой целью используются такие лекарственные препараты, как ингибиторы ангиотензин-превра-щающего фермента или антагонисты ангио-тензина II.
В начале 80-х годов XX века основной причиной этой патологии считали различные формы гломерулонефрита. В последнее время среди ведущих причин заболевания основную роль отводят сахарному диабету и артериальной гипертонии, на долю которых приходится около 70% всех случаев хронической почечной недостаточности.
Избыточная масса тела (ожирение) является наиболее важным фактором риска развития двух заболеваний — диабета и гипертонии, приводящих к терминальной стадии хронической почечной недостаточности. В нашей статье о сахарном диабете обсуждается вопрос о тесной связи диабета II типа с ожирением: около 90% всех случаев сахарного диабета возникает у лиц с избыточной массой тела.
С ее увеличением связывают и основную причину артериальной гипертонии, отводя ожирению роль фактора существенного (65-75%) риска в развитии заболевания у взрослых. Фактор избыточной массы тела, помимо нарушений функции почек, связанных с диабетом и гипертонией, способен оказывать дополнительное или си-нергическое воздействие, угнетая деятельность почек у больных на фоне уже существующей почечной патологии.
Источник

