Гипертония при аортальном стенозе
Г.Е. ГЕНДЛИН, профессор, доктор медицинских наук
О.А. ТРОНИНА, ассистент, кандидат медицинских наук
А.И. МУРСАЛИМОВА, аспирант
Кафедра госпитальной терапии № 2 РГМУ им. Н.И. Пирогова
С тех пор, как аортальный стеноз (АС) был впервые описан Стоуком в 1845 г. и Менкебергом в 1904 г., произошло резкое увеличение случаев этой болезни. Сегодня АС является третьим по распространенности в развитых странах заболеванием сердца после артериальной гипертензии (АГ) и коронарной болезни. В то же время, согласно опубликованным данным в издании Euro Heart Survey on Valvular Heart Disease, АС составляет 43% от всех клапанных заболеваний сердца.
Самой частой причиной АС среди взрослых пациентов является кальцинирование нормального трехстворчатого клапана или врожденного двухстворчатого аортального клапана.
Распространенность увеличивается с возрастом
Факторы риска развития кальцинированного АС были схожи с таковыми для развития атеросклероза. Распространенность АС устойчиво увеличивается с возрастом, составляя 15—20% у лиц старше 80 лет. Понятно, что в этой же возрастной группе велико количество больных артериальной гипертензией. Следовательно, в указанной популяции эти два заболевания могут сочетаться. АГ обнаружена у одной трети больных с симптоматическим АС. При сочетании АГ и кальцинированного АС гипертензия может оказывать влияние на клиническую картину и оценку тяжести АС, причем в этом случае стеноз аортального клапана может препятствовать лечению АГ.
Таким образом, одно заболевание может маскировать течение другого. По литературным данным, нераспознанность аортальных пороков сердца составляет 72,3%, что обусловлено, с одной стороны, недостаточной оценкой распространенности данного порока в популяции, с другой — большим количеством ассоциированных клинических состояний: АГ (89,7%), хроническими формами ИБС (80,7%), нарушениями ритма и проводимости (49,4%), перенесенными острыми нарушениями мозгового кровообращения в анамнезе (12,9%).
В одном исследовании были проспективно исследованы 5621 пациент, где изучалось влияние возраста, пола, курения, гиперлипидемии, гипертензии и ожирения на развитие кальцинированного аортального стеноза (табл.). Было показано, что АГ как важный фактор риска развития АС следует по значимости сразу после пожилого возраста, мужского пола и курения.
Является ли гипертония предиктором плохого прогноза при аортальном стенозе?
На фоне ухудшается динамика потока крови, что вызывает поражение аортального клапана в области наиболее чувствительной к давлению. Дефект эндотелия в этом регионе представляет собой основную точку приложения, где происходит инициация оксидантного стресса и воспалительных процессов.
Увеличение артериального давления может приводить к росту периферического сопротивления и снижению сосудистого комплаенса. Согласно этому имеется вероятность, что АГ может влиять на время возникновения и тяжесть симптомов АС.
Antonini—Canterin et al. (2003) обнаружили, что клинические симптомы и функ-циональный класс по NYHA были схожими у больных АС с АГ и без нее. В этом исследовании было продемонстрировано, что у пациентов с АС, сочетающимся с гипертензией, симптомы появлялись на более ранних стадиях заболевания. Из-за отсутствия надежных признаков различий в структуре ремоделирования левого желудочка у гипертоников и нормотоников представляется трудным понять, каким образом АГ вызывала более раннее развитие симптомов АС.
Этот факт объяснялся тем, что проявления АС не были «непрерывными переменными», определяемыми гипертрофией левого желудочка, — пароксизмальный рост артериального давления вместе с неожиданным увеличением постнагрузки вызывал симптомы острой сердечной недостаточности, стенокардии или синкопе.
В этом же исследовании было показано, что АГ приводила к более ранним клиническим проявлениям АС, и был сделан вывод, что наличие симптомов гипертонии у пациентов с АС является предиктором плохого прогноза у таких больных. Подобное заключение не может быть принято безоговорочно, так как оценка реального воздействия АГ на прогноз пациентов с АС требует особых методологических подходов, и более информативными являются проспективные, нежели ретроспективные исследования.
Факторы риска развития кальцинированного АС были схожи с таковыми для развития атеросклероза. Распространенность АС устойчиво увеличивается с возрастом, составляя 15–20% у лиц старше 80 лет. Понятно, что в этой же возрастной группе велико количество больных артериальной гипертензией. Следовательно, в указанной популяции эти два заболевания могут сочетаться. АГ обнаружена у одной трети больных с симптоматическим АС.
Согласно исследованию Ivanovi? et al. (2010) раннее появление симптомов АГ не являлось предиктором плохого прогноза, если симптомы, сопровождались увеличением постнагрузки.
Kadem L. et al. (2005) указали на более частую встречаемость коронарной болезни сердца у пациентов с АС и АГ по сравнению с нормотензивными больными c таким же клапанным пороком сердца (57% vs 33%, p
Гипертрофия выявляется у 100% пациентов
Клинические проявления АГ у пациентов с АС могут быть вызваны ригидностью артерий, периферическим аортальным сопротивлением, отражением пульсовых волн и постстенотической дилатацией аорты. Соответственно АГ может изменить физикальные данные при АС особенно у пожилых пациентов, у которых увеличена ригидность центральных артерий, повышено сопротивление аорты и имеется раннее появление волн отражения. II тон у таких больных может оставаться неизмененным, а интенсивность систолического шума снижена вплоть до его исчезновения, так как повышение АД снижает перепад давления на клапане.
Доказано, что наличие признаков гипертрофии ЛЖ на ЭКГ связано увеличенным кардиоваскулярным риском. Понятно, что оба представленных заболевания вызывают гипертрофию миокарда ЛЖ, что само по себе является фактором плохого прогноза.
Гипертрофия миокарда левого желудочка сердца, с учетом наличия у подавляющего большинства пациентов (78%) ассоциированных клинических состояний, выявляется в 100% случаев. Увеличение относительной толщины стенки ЛЖ сочетается с повышением фракции выброса, снижением числа желудочковых нарушений ритма и перенесенным инфарктом миокарда, уменьшением размеров полостей левых отделов сердца. Это указывает на адаптивный характер концентрического ремоделирования у подобных пациентов, что имеет место как в случае АС, так и при АГ.
Левый желудочек поражается двумя путями
При сочетании АС и АГ левый желудочек поражается двумя путями: клапанным (АС) и васкулярным (системная гипертензия). В нескольких исследованиях было обнаружено, что не существует значимой разницы в ремоделировании ЛЖ у нормотензивных больных и гипертоников с АС. Механическая обструкция аортального клапана при АС играет более значимую роль в развитии ремоделирования и гипертрофии ЛЖ, нежели АГ. В то же время некоторые исследователи исключили воздействие АГ на диастолическую и систолическую функцию ЛЖ у пациентов с АС.
Роль АГ заключается в изменении в динамикие потока крови, что вызывает поражение аортального клапана в области, наиболее чувствительной к давлению. Дефект эндотелия в этом регионе представляет собой основную точку приложения, где происходит инициация оксидантного стресса и воспалительных процессов.
Определение среднего градиента давления и площади аорты используется в качестве основных показателей в оценке тяжести АС. Увеличение артериального давления может привести к увеличению периферического сосудистого сопротивления и уменьшению сосудистой податливости и соответственно замедлить аортальный трансвальвулярный поток, что может снизить эффективность оценки тяжести АС.
Laskey et al. (1995) показали, что увеличение периферического сосудистого сопротивления приводит к снижению градиента давления и тяжести АС. Многими исследователями эти данные ставятся под сомнение, так как было показано, что существует непосредственное влияние повышенного артериального давления на гемодинамические показатели при оценке тяжести АС, в то время как другая группа исследователей оспаривала такое действие.
Увеличение аортального отверстия остается неясным феноменом
В исследовании Kadem et al. (2005) было продемонстрировано, что при субаортальном стенозе увеличение системного давления является следствием снижения градиента давления и увеличения площади аортального отверстия, которое остается до конца неясным феноменом. Возможно, расширение аорты вызывается ростом давления, что и приводит к увеличению площади отверстия аорты при АС.
Напротив, в другом исследовании in vitro показали, что системное давление приводит к небольшому линейному росту давления на биологическом протезе.
C другой стороны, исследователи показали, что площадь аортального отверстия уменьшалась при неизмененном среднем градиенте на аортальном клапане. Изменения уровня артериального давления обратно коррелировали с площадью аортального отверстия. Хотя единственным предиктором уменьшения площади аортального отверстия являлось изменение сердечного выброса.
Быстрый рост артериального давления (АД) влияет на оценку тяжести аортального стеноза. Оценка действия АГ на тяжесть течения АС чаще основывалась на определении изменения сердечного выброса и в меньшей степени на измерении увеличения периферического сосудистого сопротивления и податливости артерий.
Хроническое увеличение артериального давления отрицательно влияет на сердечно-сосудистую систему, а кальцинированный аортальный стеноз может быть не единственным клапанным пороком. Манифестация атеросклероза ухудшает различные компоненты сосудистого ложа, что предположительно определяет постнагрузку на ЛЖ. Поэтому измерение глобальной постнагрузки на ЛЖ может быть использовано в качестве предиктора систолической дисфункции ЛЖ и риска смерти у пациентов с АС.
Mascherbauer et al. (2008) в своем исследовании использовали модель кровообращения в выявлении влияния уровня систолического давления на определение площади аортального отверстия аортального клапана и трансвавулярного градиента. Авторы показали, что АД само по себе не изменяет перепад давления на клапане и не влияет на измеряемую площадь отверстия аортального клапана. Сходные результаты были получены при использовании допплерэхокардиографии и катетеризации. Эти результаты были подтверждены компьютерными анализами динамики жидкостных сред, что исключило влияние системного давления на оценку тяжести АС.
В вышеизложенных работах также исследовали влияние быстрого подъема артериального давления на тяжесть АС. В то же время хроническое увеличение артериального давления отрицательно влияет на сердечно-сосудистую систему, а кальцинированный аортальный стеноз может быть не единственным клапанным пороком. Манифестация атеросклероза ухудшает различные компоненты сосудистого ложа, что предположительно определяет постнагрузку на ЛЖ. В этом исследовании показано, что измерение глобальной постнагрузки на ЛЖ может быть использовано в качестве предиктора систолической дисфункции ЛЖ и риска смерти у пациентов с АС.
При сочетанном течении этих заболеваний
Учитывая тот факт, что патоморфология дегенеративного поражения клапанов имеет много черт, сходных с атероскле-розом, большие надежды возлагались на возможность применения статинов у таких пациентов для замедления темпов прогрессирования порока. Однако большие проспективные исследования не продемонстрировали значимого снижения темпов прогрессирования порока на фоне применения статинов.
При сочетанном течении этих двух нозологических единиц существуют определенные трудности при применении гипотензивных препаратов, что несомненно требует более тщательного контроля уровня АД у таких больных. В течение многих лет препараты группы ингибиторы АПФ относили к противопоказанному, по мнению ряда авторов, классу препаратов выбора у пациентов со стенозом клапанов сердца. В последние годы в литературе появились данные о возможной безопасности применения этой группы препаратов у таких больных, поскольку прием иАПФ снижает прогрессирование систолической дисфункции, гипертрофии миокарда ЛЖ, а также улучшает диастолическую дисфункцию.
Препараты блокаторы кальциевых каналов второго поколения не снижают финкцию ЛЖ, поэтому могут быть применены у больных с АС.
Диуретические препараты рекомендуют использовать с осторожностью. Это обусловлено прежде всего снижением объема циркулирующей крови, что особенно опасно для пожилых пациентов.
Увеличение артериального давления может приводить к росту периферического сопротивления и снижению сосудистого комплаенса. Согласно этому имеется вероятность, что АГ может влиять на время возникновения и тяжесть симптомов АС.
Единственный радикальный метод лечения
На сегодняшний день единственным радикальным методом лечения АС является хирургическое вмешательнство — протезирование аортального клапана (ПАК).
По результатам исследования Gaudino et al. (2004) стало очевидным, что АГ оказывает отрицательное действие на уменьшение индекса массы миокарда (ИММ) у пациентов после ПАК. У гипертоников с АС в первые 6 месяцев после операции отмечалось незначительное уменьшение ИММ, значение которого впоследствии возвращалось к исходному (или даже увеличивалось).
АГ изменяет течение АС, ее влияние на прогноз этих больных окончательно неизвестно. Из вышесказанного понятно, что пожилые больные с АС и АГ требуют особого подхода: интенсивного наблюдения и лечения, в том числе в ближайшем и отдаленном послеоперационных периодах после ПАК. Окончательные выводы о пользе антигипертензивного лечения этих больных, в том числе оперированных, остаются неизвестными и требуют дальнейшего изучения.
Источник
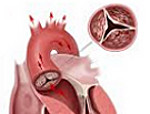
Аортальный стеноз – сужение отверстия аорты в области клапана, затрудняющее отток крови из левого желудочка. Аортальный стеноз в стадии декомпенсации проявляется головокружением, обмороками, быстрой утомляемостью, одышкой, приступами стенокардии и удушья. В процессе диагностики аортального стеноза учитываются данные ЭКГ, эхокардиографии, рентгенографии, вентрикулографии, аортографии, катетеризации сердца. При аортальном стенозе прибегают к баллонной вальвулопластике, протезированию аортального клапана; возможности консервативного лечения при данном пороке весьма ограничены.
Общие сведения
Аортальный стеноз или стеноз устья аорты характеризуется сужением выносящего тракта в области полулунного клапана аорты, в связи с чем затрудняется систолическое опорожнение левого желудочка и резко возрастает градиент давления между его камерой и аортой. На долю аортального стеноза в структуре других пороков сердца приходится 20–25%. Стеноз устья аорты в 3–4 раза чаще выявляется у мужчин, чем у женщин. Изолированный аортальный стеноз в кардиологии встречается редко – в 1,5-2% наблюдений; в большинстве случаев данный порок сочетается с другими клапанными дефектами — митральным стенозом, аортальной недостаточностью и др.
Аортальный стеноз
Классификация аортального стеноза
По происхождению различают врожденный (3-5,5%) и приобретенный стеноз устья аорты. С учетом локализации патологического сужения аортальный стеноз может быть подклапанным (25-30%), надклапанным (6-10%) и клапанным (около 60%).
Степень выраженности аортального стеноза определяется по градиенту систолического давления между аортой и левым желудочком, а также площади клапанного отверстия. При незначительном аортальном стенозе I степени площадь отверстия составляет от 1,6 до 1,2 см² (при норме 2,5—3,5 см²); градиент систолического давления находится в пределах 10–35 мм рт. ст. Об умеренном аортальном стенозе II степени говорят при площади клапанного отверстия от 1,2 до 0,75 см² и градиенте давления 36–65 мм рт. ст. Тяжелый аортальный стеноз III степени отмечается при сужении площади клапанного отверстия менее 0,74 см² и увеличении градиента давления свыше 65 мм рт. ст.
В зависимости от степени гемодинамических нарушений аортальный стеноз может протекать по компенсированному или декомпенсированному (критическому) клиническому варианту, в связи с чем выделяется 5 стадий.
I стадия (полная компенсация). Аортальный стеноз может быть выявлен только аускультативно, степень сужения устья аорты незначительна. Больным необходимо динамическое наблюдение кардиолога; хирургическое лечение не показано.
II стадия (скрытая сердечная недостаточность). Предъявляются жалобы на быструю утомляемость, одышку при умеренной физической нагрузке, головокружение. Признаки аортального стеноза определяются по данным ЭКГ и рентгенографии, градиент давления в диапазоне 36–65 мм рт. ст., что служит показанием к хирургической коррекции порока.
III стадия (относительная коронарная недостаточность). Типично усиление одышки, возникновение стенокардии, обмороков. Градиент систолического давления превышает 65 мм рт. ст. Хирургическое лечение аортального стеноза на данной стадии возможно и необходимо.
IV стадия (выраженная сердечная недостаточность). Беспокоит одышка в покое, ночные приступы сердечной астмы. Хирургическая коррекция порока в большинстве случаев уже исключена; у некоторых больных кардиохирургическое лечение потенциально возможно, но с меньшим эффектом.
V стадия (терминальная). Неуклонно прогрессирует сердечная недостаточность, выражены одышка и отечный синдром. Медикаментозное лечение позволяет добиться лишь кратковременного улучшения; хирургическая коррекция аортального стеноза противопоказана.
Причины аортального стеноза
Приобретенный аортальный стеноз чаще всего обусловлен ревматическим поражением створок клапанов. При этом заслонки клапана деформируются, сращиваются между собой, становятся плотными и ригидными, приводя к сужению клапанного кольца. Причинами приобретенного стеноза устья аорты также могут служить атеросклероз аорты, кальциноз (обызвествление) аортального клапана, инфекционный эндокардит, болезнь Педжета, системная красная волчанка, ревматоидный артрит, терминальная почечная недостаточность.
Врожденный аортальный стеноз наблюдается при врожденном сужении устья аорты или аномалии развития — двустворчатом аортальном клапане. Врожденный порок аортального клапана обычно проявляется в возрасте до 30 лет; приобретенный – в более старшем возрасте (обычно после 60 лет). Ускоряют процесс формирования аортального стеноза курение, гиперхолестеринемия, артериальная гипертензия.
Нарушения гемодинамики при аортальном стенозе
При аортальном стенозе развиваются грубые нарушения внутрисердечной, а затем и общей гемодинамики. Это связано с затрудненным опорожнением полости левого желудочка, ввиду чего происходит значительное увеличение градиента систолического давления между левым желудочком и аортой, который может достигать от 20 до 100 и более мм рт. ст.
Функционирование левого желудочка в условиях повышенной нагрузки сопровождается его гипертрофией, степень которой, в свою очередь, зависит от выраженности сужения аортального отверстия и времени существования порока. Компенсаторная гипертрофия обеспечивает длительное сохранение нормального сердечного выброса, сдерживающего развитие сердечной декомпенсации.
Однако при аортальном стенозе достаточно рано наступает нарушение коронарной перфузии, связанное с повышением конечного диастолического давления в левом желудочке и сдавлением гипертрофированным миокардом субэндокардиальных сосудов. Именно поэтому у пациентов с аортальным стенозом признаки коронарной недостаточности появляются задолго до наступления сердечной декомпенсации.
По мере снижения сократительной способности гипертрофированного левого желудочка, уменьшается величина ударного объема и фракции выброса, что сопровождается миогенной левожелудочковой дилатацией, повышением конечного диастолического давления и развитием систолической дисфункции левого желудочка. На этом фоне повышается давление в левом предсердии и малом круге кровообращения, т. е. развивается артериальная легочная гипертензия. При этом клиническая картина аортального стеноза может усугубляться относительной недостаточностью митрального клапана («митрализацией» аортального порока). Высокое давление в системе легочной артерии закономерно приводит к компенсаторной гипертрофии правого желудочка, а затем и к тотальной сердечной недостаточности.
Симптомы аортального стеноза
На стадии полной компенсации аортального стеноза больные длительное время не ощущают заметного дискомфорта. Первые проявления связаны с сужением устья аорты приблизительно до 50% ее просвета и характеризуются одышкой при физической нагрузке, быстрой утомляемостью, мышечной слабостью, ощущением сердцебиений.
На этапе коронарной недостаточности присоединяются головокружение, обмороки при быстрой смене положения тела, приступы стенокардии, пароксизмальная (ночная) одышка, в тяжелых случаях — приступы сердечной астмы и отек легких. Прогностически неблагоприятно сочетание стенокардии с синкопальными состояниями и особенно – присоединение сердечной астмы.
При развитии правожелудочковой недостаточности отмечаются отеки, ощущение тяжести в правом подреберье. Внезапная сердечная смерть при аортальном стенозе наступает в 5–10% случаев, главным образом, у лиц пожилого возраста с выраженным сужением клапанного отверстия. Осложнениями аортального стеноза могут являться инфекционный эндокардит, ишемические нарушения мозгового кровообращения, аритмии, АВ-блокады, инфаркт миокарда, желудочно-кишечные кровотечения из нижних отделов пищеварительного тракта.
Диагностика аортального стеноза
Внешний вид больного с аортальным стенозом характеризуется бледностью кожных покровов («аортальной бледностью»), обусловленной склонностью к периферическим вазоконстрикторным реакциям; в поздних стадиях может отмечаться акроцианоз. Периферические отеки выявляются при аортальном стенозе тяжелой степени. При перкуссии определяется расширение границ сердца влево и вниз; пальпаторно ощущается смещение верхушечного толчка, систолическое дрожание в яремной ямке.
Аускультативными признаками аортального стеноза служит грубый систолический шум над аортой и над митральным клапаном, приглушение I и II тонов на аорте. Указанные изменения также регистрируются при фонокардиографии. По данным ЭКГ определяются признаки гипертрофии левого желудочка, аритмии, иногда – блокады.
В период декомпенсации на рентгенограммах выявляется расширение тени левого желудочка в виде удлинения дуги левого контура сердца, характерная аортальная конфигурация сердца, постстенотическая дилатация аорты, признаки легочной гипертензии. На эхокардиографии определяется утолщение заслонок аортального клапана, ограничение амплитуды движения створок клапана в систолу, гипертрофия стенок левого желудочка.
С целью измерения градиента давления между левым желудочком и аортой выполняется зондирование полостей сердца, которое позволяет косвенно судить о степени аортального стеноза. Вентрикулография необходима для выявления сопутствующей митральной недостаточности. Аортография и коронарография применяются для дифференциальной диагностики аортального стеноза с аневризмой восходящего отдела аорты и ИБС.
Лечение аортального стеноза
Все пациенты, в т.ч. с бессимптомным, полностью компенсированным аортальным стенозом, должны находиться под тщательным наблюдением кардиолога. Им рекомендуются проведение ЭхоКГ каждые 6-12 месяцев. Данному контингенту больных с целью профилактики инфекционного эндокардита необходим превентивный прием антибиотиков перед стоматологическими (лечение кариеса, удаление зубов и т. д.) и другими инвазивными процедурами. Ведение беременности у женщин с аортальным стенозом требует тщательного контроля показателей гемодинамики. Показанием к прерыванию беременности служит тяжелая степень аортального стеноза или нарастание признаков сердечной недостаточности.
Медикаментозная терапия при аортальном стенозе направлена на устранение аритмий, профилактику ИБС, нормализацию АД, замедление прогрессирования сердечной недостаточности.
Радикальная хирургическая коррекция аортального стеноза показана при первых клинических проявлениях порока – появлении одышки, ангинозных болей, синкопальных состояний. С этой целью может применяться баллонная вальвулопластика — эндоваскулярная балонная дилатация аортального стеноза. Однако зачастую данная процедура бывает малоэффективна и сопровождается последующим рецидивом стеноза. При негрубых изменениях створок аортального клапана (чаще у детей с врожденным пороком) используется открытая хирургическая пластика аортального клапана (вальвулопластика). В детской кардиохирургии нередко выполняется операция Росса, предполагающая пересадку клапана легочной артерии в аортальную позицию.
При соответствующих показаниях прибегают к проведению пластики надклапанного или подклапанного аортального стеноза. Основным методом лечения аортального стеноза на сегодняшний день остается протезирование аортального клапана, при котором пораженный клапан полностью удаляется и заменяется на механический аналог или ксеногенный биопротез. Пациентам с искусственным клапаном требуется пожизненный прием антикоагулянтов. В последние годы практикуется перкутанная замена аортального клапана.
Прогноз и профилактика аортального стеноза
Аортальный стеноз может протекать бессимптомно в течение многих лет. Появление клинических симптомов существенно увеличивает риск осложнений и летальности.
Основными, прогностически значимыми симптомами служат стенокардия, обмороки, левожелудочковая недостаточность – в этом случае средняя продолжительность жизни не превышает 2-5 лет. При своевременном оперативном лечении аортального стеноза 5-летняя выживаемость составляет около 85%, 10-летняя — порядка 70%.
Меры профилактики аортального стеноза сводятся к предупреждению ревматизма, атеросклероза, инфекционного эндокардита и др. способствующих факторов. Больные с аортальным стенозом подлежат диспансеризации и наблюдению кардиолога и ревматолога.
Источник

