Температура кипения при повышенном давлении
Òåìïåðàòóðà êèïåíèÿ — ýòî òåìïåðàòóðà, ïðè êîòîðîé ïðîèñõîäèò êèïåíèå æèäêîñòè, êîòîðàÿ íàõîäèòñÿ ïîä ïîñòîÿííûì äàâëåíèåì. Ñîãëàñíî óðàâíåíèþ Êëàïåéðîíà — Êëàóçèóñà ñ ðîñòîì äàâëåíèÿ òåìïåðàòóðà êèïåíèÿ óâåëè÷èâàåòñÿ, à ñ óìåíüøåíèåì äàâëåíèÿ òåìïåðàòóðà êèïåíèÿ ñîîòâåòñòâåííî óìåíüøàåòñÿ. Óçíàòü êàê òåìïåðàòóðà êèïåíèÿ âîäû áóäåò çàâèñåòü îò äàâëåíèÿ âû ñìîæåòå èç òàáëèöû.
Çíà÷åíèÿ:
- tk,°C — òåìïåðàòóðà êèïåíèÿ âîäû (°C);
- P — îáùåå äàâëåíèå;
- êÏà — êèëîïàñêàëü;
- àòì. — àòìîñôåðà.
P | tk,°C | |
êÏà. | àòì. | |
0,981 | 0,01 | 6,698 |
1,961 | 0,02 | 17,20 |
3,923 | 0,05 | 28,64 |
9,807 | 0,1 | 45,45 |
19,61 | 0,2 | 59,67 |
29,42 | 0,3 | 68,68 |
39,23 | 0,4 | 75,42 |
49,03 | 0,5 | 80,86 |
58,84 | 0,6 | 85,45 |
68,65 | 0,7 | 89,45 |
78,45 | 0,8 | 92,99 |
88,26 | 0,9 | 96,18 |
98,07 | 1,0 | 99,09 |
101,3 | 1,033 | 100,00 |
147,1 | 1,5 | 110,79 |
196,1 | 2,0 | 119,62 |
245,2 | 2,5 | 126,79 |
294,2 | 3,0 | 132,88 |
392,3 | 4,0 | 142,92 |
490,3 | 5,0 | 151,11 |
588,4 | 6,0 | 158,08 |
686,5 | 7,0 | 164,17 |
784,5 | 8,0 | 169,61 |
882,6 | 9,0 | 174,53 |
980,7 | 10,0 | 179,04 |
1961 | 20,0 | 211,38 |
2452 | 25,0 | 222,90 |
4903 | 50,0 | 262,70 |
9807 | 100,0 | 309,53 |
Êàëüêóëÿòîðû ïî ôèçèêå | |
| Ðåøåíèå çàäà÷ ïî ôèçèêå, ïîäãîòîâêà ê ÝÃÅ è ÃÈÀ, ìåõàíèêà òåðìîäèíàìèêà è äð. | |
| Êàëüêóëÿòîðû ïî ôèçèêå | |
Ôèçèêà 7,8,9,10,11 êëàññ, ÅÃÝ, ÃÈÀ | |
| Îñíîâíàÿ èíôîðìàöèÿ ïî êóðñó ôèçèêè äëÿ îáó÷åíèÿ è ïîäãîòîâêè â ýêçàìåíàì, ÃÂÝ, ÅÃÝ, ÎÃÝ, ÃÈÀ | |
| Ôèçèêà 7,8,9,10,11 êëàññ, ÅÃÝ, ÃÈÀ | |
Источник
Зависимость температуры кипения от давления
Температура кипения воды равна 100 °C; можно подумать, что это неотъемлемое свойство воды, что вода, где бы и в каких условиях она ни находилась, всегда будет кипеть при 100 °C.
Но это не так, и об этом прекрасно осведомлены жители высокогорных селений.
Вблизи вершины Эльбруса имеется домик для туристов и научная станция. Новички иногда удивляются, «как трудно сварить яйцо в кипятке» или «почему кипяток не обжигает». В этих случаях им указывают, что вода кипит на вершине Эльбруса уже при 82 °C.
В чем же тут дело? Какой физический фактор вмешивается в явление кипения? Какое значение имеет высота над уровнем моря?
Этим физическим фактором является давление, действующее на поверхность жидкости. Не нужно забираться на вершину горы, чтобы проверить справедливость сказанного.
Помещая подогреваемую воду под колокол и накачивая или выкачивая оттуда воздух, можно убедиться, что температура кипения растет при возрастании давления и падает при его уменьшении.
Вода кипит при 100 °C только при определенном давлении – 760 мм Hg.
Кривая температуры кипения в зависимости от давления показана на рис. 98. На вершине Эльбруса давление равно 0,5 атм, этому давлению и соответствует температура кипения 82 °C.
А вот водой, кипящей при 10–15 мм Нg, можно освежиться в жаркую погоду. При этом давлении температура кипения упадет до 10–15 °C.
Можно получить даже «кипяток», имеющий температуру замерзающей воды. Для этого придется снизить давление до 4,6 мм Hg.
Интересную картину можно наблюдать, если поместить открытый сосуд с водой под колокол и откачивать воздух. Откачка заставит воду закипеть, но кипение требует тепла. Взять его неоткуда, и воде придется отдать свою энергию. Температура кипящей воды начнет падать, но так как откачка продолжается, то падает и давление. Поэтому кипение не прекратится, вода будет продолжать охлаждаться и в конце концов замерзнет.
Такое кипение холодной воды происходит не только при откачке воздуха. Например, при вращении гребного корабельного винта давление в быстро движущемся около металлической поверхности слое воды сильно падает и вода в этом слое закипает, т.е. в ней появляются многочисленные наполненные паром пузырьки. Это явление называется кавитацией (от латинского слова cavitas – полость).
Снижая давление, мы понижаем температуру кипения. А увеличивая его? График, подобный нашему, отвечает на этот вопрос. Давление в 15 атм может задержать кипение воды, оно начнется только при 200 °C, а давление в 80 атм заставит воду закипеть лишь при 300 °C.
Итак, определенному внешнему давлению соответствует определенная температура кипения. Но это утверждение можно и «перевернуть», сказав так: каждой температуре кипения воды соответствует свое определенное давление. Это давление называется упругостью пара.
Кривая, изображающая температуру кипения в зависимости от давления, является одновременно и кривой упругости пара в зависимости от температуры.
Цифры, нанесенные на график температуры кипения (или на график упругости пара), показывают, что упругость пара меняется очень резко с изменением температуры. При 0 °C (т.е. 273 K) упругость пара равна 4,6 мм Hg, при 100 °C (373 K) она равна 760 мм, т. е, возрастает в 165 раз. При повышении температуры вдвое (от 0 °C, т.е. 273 K, до 273 °C, т.е. 546 K) упругость пара возрастает с 4,6 мм Hg почти до 60 атм, т.е. примерно в 10000 раз.
Поэтому, напротив, температура кипения меняется с давлением довольно медленно. При изменении давления вдвое – от 0,5 атм до 1 атм, температура кипения возрастает от 82 °C (т.е. 355 K) до 100 °C (т.е. 373 K) и при изменении вдвое от 1 атм до 2 атм – от 100 °C (т.е. 373 K) до 120 °C (т.е. 393 K).
Та же кривая, которую мы сейчас рассматриваем, управляет и конденсацией (сгущением) пара в воду.
Превратить пар в воду можно либо сжатием, либо охлаждением.
Как во время кипения, так и в процессе конденсации точка не сдвинется с кривой, пока превращение пара в воду или воды в пар не закончится полностью. Это можно сформулировать еще и так: в условиях нашей кривой и только при этих условиях возможно сосуществование жидкости и пара. Если при этом не подводить и не отнимать тепла, то количества пара и жидкости в закрытом сосуде будут оставаться неизменными. Про такие пар и жидкость говорят, что они находятся в равновесии, и пар, находящийся в равновесии со своей жидкостью, называют насыщенным.
Кривая кипения и конденсации имеет, как мы видим, еще один смысл – это кривая равновесия жидкости и пара. Кривая равновесия делит поле диаграммы на две части. Влево и вверх (к большим температурам и меньшим давлениям) расположена область устойчивого состояния пара. Вправо и вниз – область устойчивого состояния жидкости.
Кривая равновесия пар – жидкость, т.е. кривая зависимости температуры кипения от давления или, что то же самое, упругости пара от температуры, примерно одинакова для всех жидкостей. В одних случаях изменение может быть несколько более резким, в других – несколько более медленным, но всегда упругость пара быстро растет с увеличением температуры.
Уже много раз мы пользовались словами «газ» и «пар». Эти два слова довольно равноправны. Можно сказать: водяной газ есть пар воды, газ кислород есть пар кислородной жидкости. Все же при пользовании этими двумя словами сложилась некоторая привычка. Так как мы привыкли к определенному относительно небольшому интервалу температур, то слово «газ» мы применяем обычно к тем веществам, упругость пара которых при обычных температурах выше атмосферного давления. Напротив, о паре мы говорим тогда, когда при комнатной температуре и давлении атмосферы вещество более устойчиво в виде жидкости.
Следующая глава >
Содержание >
Похожие главы из других книг
К квантовой теории абсолютного нуля температуры
Д. Бак, Г. Бете, В. Рицлер
(Кембридж)
«К квантовой теории абсолютного нуля температуры» и заметки, переводы которых помещены ниже:
К квантовой теории абсолютного нуля температуры
Движение нижней челюсти у крупного
К квантовой теории абсолютного нуля температуры
Ниже помещен перевод заметки» написанной известными физиками и опубликованной в «Natur-wissenschaften». Редакторы журнала «попались на удочку громких имен» и, не вдаваясь в существо написанного, направили полученный материал в
6. Математическая статистика и корреляционная зависимость
Математическая статистика – наука о математических методах систематизации и использования статистических данных для решения научных и практических задач. Математическая статистика тесно примыкает к теории
Изменение давления с высотой
С изменением высоты давление падает. Впервые это было выяснено французом Перье по поручению Паскаля в 1648 г. Гора Пью де Дом, около которой жил Перье, была высотой 975 м. Измерения показали, что ртуть в торричеллиевой трубке падает при подъеме на
Влияние давления на температуру плавления
Если изменить давление, то изменится и температура плавления. С такой же закономерностью мы встречались, когда говорили о кипении. Чем больше давление, тем выше температура кипения. Как правило, это верно и для плавления. Однако
Источник
Из приведенных
рассуждений ясно, что температура
кипения жидкости должна зависеть от
внешнего давления. Наблюдения подтверждают
это.
Чем
больше внешнее давление, тем выше
температура кипения. Так, в паровом
котле при давлении, достигающем 1,6 · 106
Па, вода не кипит и при температуре 200
°С. В медицинских учреждениях кипение
воды в герметически закрытых сосудах
— автоклавах (рис. 6.11) также происходит
при повышенном давлении. Поэтому
температура кипения значительно выше
100 °С. Автоклавы применяют для стерилизации
хирургических инструментов, перевязочного
материала и т. д.
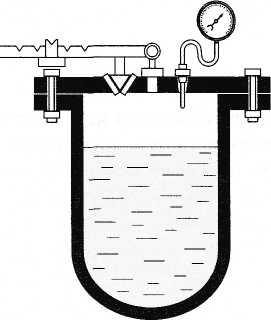
Рис. 6.11
И
наоборот, уменьшая внешнее давление,
мы тем самым понижаем температуру
кипения. Под колоколом воздушного насоса
можно заставить воду кипеть при комнатной
температуре (рис. 6.12). При подъеме в горы
атмосферное давление уменьшается,
поэтому уменьшается температура кипения.
На высоте 7134 м (пик Ленина на Памире)
давление приближенно равно 4 · 104
Па (300 мм рт. ст.). Вода кипит там примерно
при 70 °С. Сварить, например, мясо в этих
условиях невозможно.
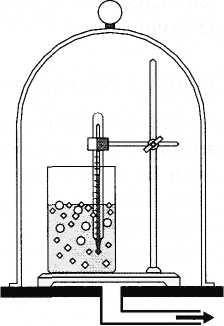
Рис. 6.12
На рисунке 6.13
изображена кривая зависимости температуры
кипения воды от внешнего давления. Легко
сообразить, что эта кривая является
одновременно и кривой, выражающей
зависимость давления насыщенного
водяного пара от температуры.
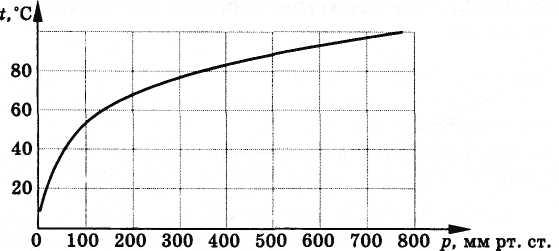
Рис. 6.13
Различие температур кипения жидкостей
У каждой жидкости
своя температура кипения. Различие
температур кипения жидкостей определяется
различием в давлении их насыщенных
паров при одной и той же температуре.
Например, пары эфира уже при комнатной
температуре имеют давление, большее
половины атмосферного. Поэтому, чтобы
давление паров эфира стало равным
атмосферному, нужно небольшое повышение
температуры (до 35 °С). У ртути же насыщенные
пары имеют при комнатной температуре
совсем ничтожное давление. Давление
паров ртути делается равным атмосферному
только при значительном повышении
температуры (до 357 °С). Именно при этой
температуре, если внешнее давление
равно 105 Па, и кипит ртуть.
Различие температур
кипения веществ находит большое
применение в технике, например при
разделении нефтепродуктов. При нагревании
нефти раньше всего испаряются наиболее
ценные, летучие ее части (бензин), которые
можно таким образом отделить от «тяжелых»
остатков (масел, мазута).
Жидкость закипает,
когда давление ее насыщенного пара
сравнивается с давлением внутри жидкости.
§ 6.6. Теплота парообразования
Требуется ли
энергия для превращения жидкости в пар?
Скорее всего да! Не так ли?
Мы отмечали (см. §
6.1), что испарение жидкости сопровождается
ее охлаждением. Для поддержания
температуры испаряющейся жидкости
неизменной к ней необходимо подводить
извне теплоту. Конечно, теплота и сама
может передаваться жидкости от окружающих
тел. Так, вода в стакане испаряется, но
температура воды, несколько более
низкая, чем температура окружающего
воздуха, остается неизменной. Теплота
передается от воздуха к воде до тех пор,
пока вся вода не испарится.
Чтобы поддерживать
кипение воды (или иной жидкости), к ней
тоже нужно непрерывно подводить теплоту,
например подогревать ее горелкой. При
этом температура воды и сосуда не
повышается, но каждую секунду образуется
определенное количество пара.
Таким
образом, для превращения жидкости в пар
путем испарения или путем кипения
требуется приток теплоты. Количество
теплоты, требующееся для превращения
данной массы жидкости в пар той же
температуры, называется теплотой
парообразования этой жидкости.
На что расходуется
подводимая к телу энергия? Прежде всего
на увеличение его внутренней энергии
при переходе из жидкого состояния в
газообразное: ведь при этом увеличивается
объем вещества от объема жидкости до
объема насыщенного пара. Следовательно,
увеличивается среднее расстояние между
молекулами, а значит, и их потенциальная
энергия.
Кроме того, при
увеличении объема вещества совершается
работа против сил внешнего давления.
Эта часть теплоты парообразования при
комнатной температуре составляет обычно
несколько процентов всей теплоты
парообразования.
Теплота
парообразования зависит от рода жидкости,
ее массы и температуры. Зависимость
теплоты парообразования от рода жидкости
характеризуется величиной, называемой
удельной
теплотой парообразования.
Удельной теплотой
парообразования данной жидкости
называется отношение теплоты
парообразования жидкости к ее массе:
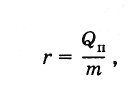 (6.6.1)
(6.6.1)
где
r
— удельная теплота парообразования
жидкости; т
—
масса жидкости; Qn
— ее теплота парообразования. Единицей
удельной теплоты парообразования в СИ
является джоуль
на килограмм (Дж/кг).
Удельная
теплота парообразования воды очень
велика: 2,256·106
Дж/кг при температуре 100 °С. У других
жидкостей (спирт, эфир, ртуть, керосин
и др.) удельная теплота парообразования
меньше в 3—10 раз.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Для чего человек начал кипятить воду перед её непосредственным употреблением? Правильно, чтобы обезопасить себя от многих болезнетворных бактерий и вирусов. Эта традиция пришла на территорию средневековой России ещё до Петра Первого, хотя считается, что именно он завёз первый самовар в страну и ввёл обряд неспешного вечернего чаепития. На самом деле некое подобие самоваров наш народ использовал ещё в древней Руси для приготовления напитков из трав, ягод и корений. Кипячение требовалось здесь в основном для извлечения полезных экстрактов растений, нежели для обеззараживания. Ведь в ту пору даже не было известно о микромире, где эти бактерии с вирусами обитают. Однако благодаря кипячению нашу страну обходили стороной мировые пандемии страшных заболеваний, таких как холера или дифтерия.

Шкала Цельсия
Великий метеоролог, геолог и астроном из Швеции Андерс Цельсий изначально использовал значение в 100 градусов для обозначения точки замерзания воды при нормальных условиях, а температура кипения воды была принята за нуль градусов. И уже после его смерти в 1744 году не менее известная личность, ботаник Карл Линней и приемник Цельсия Мортен Штремер, перевернули эту шкалу для удобства её использования. Однако, по другим сведениям, это сделал сам Цельсий незадолго до своей кончины. Но в любом случае стабильность показаний и понятная градуировка повлияли на повсеместное распространение её использования среди самых престижных на то время научных профессий — химиков. И, несмотря на то что в перевернутом виде отметка шкалы в 100 градусов устанавливала точку стабильного кипения воды, а не начала её замерзания, шкала стала носить имя первостепенного её создателя, Цельсия.
Ниже атмосферы
Однако не всё так просто, как кажется на первый взгляд. Взглянув на любую диаграмму состояния в P-T- или P-S-координатах (энтропия S функциональна от температуры в прямой зависимости), мы увидим, как тесно связаны между собой температура и давление. Так же и температура кипения воды в зависимости от давления меняет свои значения. И любому альпинисту прекрасно знакомо это свойство. Каждый, кто хоть раз в жизни постигал высоты свыше 2000-3000 метров над уровнем моря, знает, насколько тяжело дышится на высоте. Это из-за того, что чем выше мы поднимаемся, тем разреженнее становится воздух. Атмосферное давление падает ниже одной атмосферы (ниже н. у., то есть ниже «нормальных условий»). Падает и температура кипения воды. В зависимости от давления на каждой из высот она может закипать как при восьмидесяти, так и при шестидесяти градусах Цельсия.

Скороварки
Однако следует помнить, что хоть основные микробы и погибают при температурах выше шестидесяти градусов Цельсия, многие могут выжить при восьмидесяти и более градусах. Именно поэтому мы добиваемся кипячения воды, то есть доводим её температуру до 100 °С. Однако есть интересные кухонные приборы, позволяющие сократить время и нагреть жидкость до высоких температур, без её кипячения и потери массы посредством испарения. Понимая, что температура кипения воды в зависимости от давления может изменяться, инженеры из США на основе французского прототипа представили миру в 1920-х годах скороварку. Принцип её действия основан на том, что крышка плотно прижимается к стенкам, без возможности отвода пара. Внутри создаётся повышенное давление, и вода закипает при более высоких температурах. Однако такие девайсы довольно опасны и нередко приводили к взрыву и серьёзным ожогам пользователей.
В идеале
Давайте рассмотрим, как наступает и проходит сам процесс. Вообразим себе идеально гладкую и бесконечно большую поверхность нагрева, где распределение теплоты происходит равномерно (к каждому квадратному миллиметру поверхности подводится одинаковое количество тепловой энергии), а коэффициент шероховатости поверхности стремится к нулю. В этом случае при н. у. кипение в ламинарном погранслое будет начинаться одновременно по всей площади поверхности и происходить моментально, сразу испаряя весь единичный объём жидкости, находящейся на её поверхности. Это идеальные условия, в реальной жизни такого не бывает.

В реальности
Давайте выясним, какова начальная температура кипения воды. В зависимости от давления она тоже меняет свои значения, однако основной момент здесь кроется вот в чём. Если даже мы возьмём самую гладкую, на наш взгляд, кастрюлю и поднесём её под микроскоп, то в его окуляре мы увидим неравномерные края и острые частые пики, выступающие над основной поверхностью. Теплота к поверхности кастрюли, будем считать, подводится равномерно, хотя в реальности это тоже не совсем верное утверждение. Даже когда кастрюля стоит на самой крупной конфорке, на плите градиент температур распределяется неравномерно, и всегда существуют локальные зоны перегрева, отвечающие за раннее кипение воды. Сколько градусов при этом на пиках поверхности и в её низинах? Пики поверхности при бесперебойном подведении теплоты прогреваются быстрее низин и так называемых впадин. Более того, окруженные со всех сторон водой с низкой температурой, они лучше отдают энергию молекулам воды. Коэффициент температуропроводности пиков в полтора-два раза выше, чем у низин.

Температуры
Именно поэтому начальная температура кипения воды составляет порядка восьмидесяти градусов Цельсия. При этом значении пики поверхности подводят достаточное количество теплоты, необходимого для мгновенного вскипания жидкости и образования первых пузырьков, видимых глазу, которые робко начинают подниматься к поверхности. А какова температура кипения воды при нормальном давлении — спрашивают многие. Ответ на этот вопрос можно без труда найти в таблицах. При атмосферном давлении стабильное кипение устанавливается при 99,9839 °С.
Источник


