Патогенез гипертонии при сахарном диабете
Существуют наиболее частые причины развития АГ при сахарном диабете.

Основные причины развития АГ при СД
Из приведенных данных видно, что основной причиной развития АГ при СД типа I является диабетическое поражение почек, при СД типа 2 — гипертоническая болезнь и изолированная систолическая гипертония.
К эндокринным причинам относятся: тиреотоксикоз, гипотиреоз, гиперкортицизм, альдостерома, феохромоцитома, акромегалия.
Необходимо помнить также о том, что АГ при СД может быть индуцирована злоупотреблением алкоголя или приемом некоторых лекарственных препаратов, повышающих АД, — глюкокортикоидов, контрацептивов.
Патогенез АГ при СД типа 1
При СД типа 1 генез АГ на 80-90 % связан с развитием ДН. Она наблюдается у 35-40 % больных СД типа 1 и проходит несколько стадий: стадия МАУ, стадия ПУ и стадия ХПН. Повышение АД (> 130/80 мм рт. ст.) выявляется у 20 % больных с МАУ, у 70 % — на стадии ПУ и у 95-100 % — на стадии ХПН. В наших исследованиях отмечена высокая корреляция между уровнем экскреции белка с мочой и степенью повышения АД. Коэффициент корреляции АД с МАУ составил 0,62 (р <0,015), АД с ПУ — 0,60 (р <0,012).
Ведущий механизм развития АГ при ДН связан с повышенной реабсорбцией натрия в почечных канальцах и низкой экскрецией натрия с мочой, вследствие чего в организме приблизительно на 10 % по сравнению с нормой возрастает концентрация ионообменного натрия. Вместе с натрием во вне- и внутриклеточном пространствах накапливается жидкость. Развивается гиперволемия, ведущая к увеличению сердечного выброса. Гипергликемия, поддерживая высокую осмолярность крови, также способствует развитию гиперволемии. Следовательно, АГ при СД типа 1 носит Na-зависимый и объемзависимый характер.

Патогенез АГ при СД типа 1
Снижение почечной экскреции натрия при СД типа 1 происходит вследствие нескольких причин:
• повышенной реабсорбции глюкозы в почечных канальцах, сопряженной с реабсорбцией натрия;
• высокой активности локально-почечного ангиотензина II, стимулирующего реабсорбцию натрия;
• сниженной чувствительности почечных канальцев к предсердному натрийуретическому фактору;
• сниженной активности других натрийуретических факторов (простагландины, калликреин).
Повышение содержания натрия и сопряженное с ним накопление ионов Са;+ в стенках сосудов увеличивают аффинность рецепторов сосудов к катехоламинам и другим констрикторным гормонам (ангиотензину II (AT II), эндотелину-1), что способствует спазму сосудов и повышению общего периферического сопротивления сосудов (ОПСС).
Центральную роль в регуляции тонуса сосудов и водно-солевого гомеостаза при СД типа 1 играет активность локально-почечной ренин-ангиотензиновой системы (РАС). Даже на самых ранних стадиях ДН (при появлении МАУ) уже отмечается высокая активность РАС, Гиперпродукция локально-почечного AT II вызывает многочисленные патологические эффекты: системную АГ, внутриклубочковую гипертензию, что ускоряет прогрессирование диабетического гломерулосклероза; оказывает стимулирующее рост и митогенное действие, что способствует склерозированию почечной ткани, развитию патологии сердечной мышцы и формированию атеросклеротического ремоделирования сосудов.
Экспериментальные и клинические данные о патогенной роли РАС в формировании АГ и сосудистых осложнений СД подтверждаются высокой антигипертензивной и органопротективной эффективностью препаратов, блокирующих активность РАС, — ингибиторов ангиотензинпревращающего фермента (иАПФ) и антагонистов рецепторов к АТП.
Патогенез АГ при СД типа 2
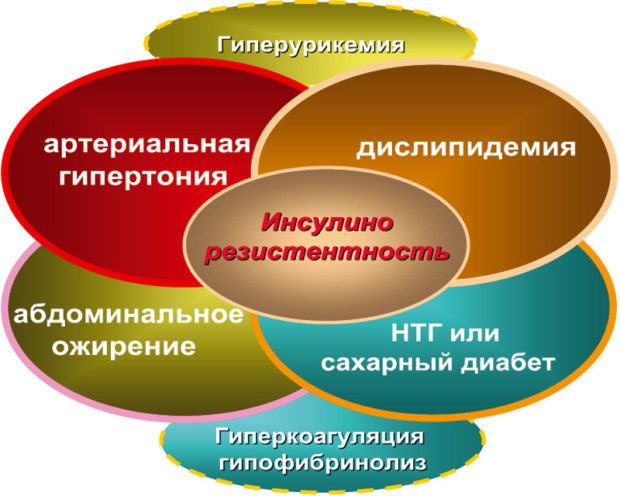
Синдром инсулинорезистентности. АГ при СД типа 2 является составляющей синдрома ИР (или метаболического синдрома), описанного в 1988 г. G. М. Reaven. Термин «метаболический синдром» в настоящее время объединяет СД типа 2 (или НТГ), АГ, дислипидемию (в основном — гипертриглицеридемию), абдоминальное ожирение, типерурикемию, МАУ и повышенное содержание в крови прокоагулянтов (фибриногена, ингибитора активатора плазминогена 1). Все перечисленные состояния являются следствием сниженной чувствительности периферических тканей к инсулину, т. е. ИР. Последняя встречается и при других патологических или физиологических состояниях, не входящих в понятие метаболический синдром: поликистоз яичников, ХПН, инфекции, терапия глюкокортикоидами, беременность, старение.
Распространенность ИР изучена в крупном популяционном исследовании, проведенном в Италии, включавшем 888 человек в возрасте от 40 до 79 лет.
При анализе ИР методом НОМА было выявлено, что она встречается у:
— 10 % лиц без метаболических нарушений;
— 58 % лиц с эссенциальной АГ (АД > 160/95 мм рт. ст.);
— 63 % лиц с гиперурикемией (содержание мочевой кислоты в сыворотке крови > 416 мкмоль/л у мужчин и > 387 мкмоль/л у женщин);
— 84 % лиц с гипертриглицеридемией (ТГ > 2,85 ммоль/л);
— 88 % лиц с низким уровнем ХС ЛПВП (< 0,9 ммоль/л у мужчин и < 1,0 у женщин);
— 66 % лиц с НТГ;
— 84% лиц с СД типа 2 (при его диагностике по критериям: гликемия натощак > 7,8 ммоль/л и через 2 ч после нагрузки глюкозой >11,1 ммоль/л).
При сочетании СД типа 2 (или НТГ) с дислипидемией, гиперурикемией и АГ, т. е. с основными компонентами метаболического синдрома, частота выявления ИР составляла 95 %. Это свидетельствует о том, что, действительно, ведущим механизмом развития метаболического синдрома является ИР.
Роль ИР в развитии СД типа 2
ИР периферических тканей лежит в основе развития СД типа 2. Наибольшее клиническое значение имеет потеря чувствительности к инсулину мышечной, жировой и печеночной тканей. ИР мышечной ткани проявляется в снижении поступления глюкозы из крови в миоциты и ее утилизации в мышечных клетках, жировой ткани — в резистентности к антилиполитическому действию инсулина, проводящему к накоплению свободных жирных кислот (СЖК) и глицерина. СЖК поступают в печень, где становятся основным источником образования атерогенных липопротеинов очень низкой плотности (ЛПОНП). ИР ткани печени характеризуется сниженным синтезом гликогена и активацией распада гликогена до глюкозы (гликогенолиз) и синтеза глюкозы de novo из аминокислот, лактата, пирувата, глицерина (глюконеогенез), в результате чего глюкоза из печени поступает в кровоток. Эти процессы в печени активируются вследствие отсутствия их подавления инсулином.
ИР периферических тканей предшествует развитию СД типа 2 и может выявляться у ближайших родственников больных СД типа 2, не имеющих нарушений углеводного обмена. Долгое время ИР компенсируется избыточной продукцией инсулина β-клетками поджелудочной железы (гиперинсулинемией), что поддерживает углеводный обмен в норме. Гиперинсулинемия приравнивается к маркерам ИР и считается предвестником СД типа 2. Впоследствии при нарастании степени ИР β-клетки перестают справляться с увеличившейся нагрузкой глюкозой, что приводит к постепенному истощению инсулинсекреторной способности и клинической манифестации СД. В первую очередь страдает 1-я фаза секреции инсулина (быстрая) в ответ на пищевую нагрузку, 2-я фаза (фаза базальной секреции инсулина) также начинает снижаться.

Стадии развития СД типа 2
Развившаяся гипергликемия еще больше усиливает ИР периферических тканей и подавляет инсулинсекреторную функцию β-клеток. Этот механизм получил название глюкозотоксичностъ.
Предполагают, что феномен ИР имеет прочную генетическую основу, закрепленную в ходе эволюции. Согласно гипотезе об «экономном генотипе», выдвинутой V. Neel в 1962 г., ИР — это эволюционно закрепленный механизм выживания в неблагоприятных условиях, когда периоды изобилия чередовались с периодами голода. Наличие ИР обеспечивало накопление энергии в виде отложений жира, запасов которого хватало на то, чтобы пережить голод. В ходе естественного отбора как наиболее целесообразные закреплялись те гены, которые обеспечивали ИР и накопление энергии. Гипотеза подтверждается в эксперименте на мышах, которых подвергали длительному голоданию. Выживали только те мыши, у которых имелась генетически опосредованная ИР. В современных условиях в странах с высоким уровнем жизни, характеризующимся гиподинамией и высококалорийным питанием, сохранившиеся в генетической памяти механизмы ИР продолжают «работать» на накопление энергии, что ведет к абдоминальному ожирению, дислипидемии, АГ и, наконец, СД типа 2.
К настоящему времени накоплено достаточно данных, позволяющих утверждать, что ИР и сопутствующая ей гиперинсулинемия являются факторами риска ускоренного атерогенеза и высокой летальности от ИБС. Недавно завершилось крупное исследование IRAS (Insulin Resistance Atherosclerosis Study), целью которого было оценить взаимосвязь между ИР (определяемой при внутривенном тесте толерантности к глюкозе) и сердечно-сосудистыми факторами риска в популяции лиц без СД и больных СД типа 2. В качестве маркера атеросклеротического поражения сосудов измерялась толщина стенки сонной артерии. В результате исследования выявлена четкая прямая зависимость между степенью ИР и выраженностью абдоминального ожирения, атерогенностью липидного спектра крови, активацией системы коагуляции, а также толщиной стенки сонной артерии как у лиц без СД, так и у больных СД типа 2. На каждую единицу ИР толщина стенки сонной артерии увеличивается на 30 мкм.
Существует немало клинических доказательств тому, что гиперинсулинемия является независимым фактором риска ИБС у лиц без СД типа 2: исследования Paris prospective (около 7000 обследованных), Busselton (более 1000 обследованных) и Helsinki Policemen (982 обследованных) (метаанализ В. Balkau и др.). В последние годы аналогичная зависимость выявлена и у больных с СД типа 2. Этим данным есть экспериментальное обоснование. Работы R. Stout свидетельствуют о том, что инсулин оказывает прямое атерогенное действие на стенки сосудов, вызывая пролиферацию и миграцию гладкомышечных клеток, синтез липидов в них, пролиферацию фибробластов, активацию свертывающей системы крови, снижение активности фибринолиза.
Таким образом, ИР и гиперинсулинемия привносят весомый вклад в прогрессирование атеросклероза как у лиц, предрасположенных к развитию СД, так и у больных СД типа 2.
Роль ИР в развитии АГ
Взаимосвязь гиперинсулинемии (маркера ИР) и эссенциальной АГ настолько прочна, что при высокой концентрации инсулина плазмы у больного можно прогнозировать развитие у него в скором времени АГ. Причем эта связь прослеживается как у больных с ожирением, так и у лиц с нормальной массой тела.
Существует несколько механизмов, объясняющих повышение АД при гиперинсулинемии. Инсулин способствует активации симпатической нервной системы, повышению реабсорбции Na и жидкости в почечных канальцах, внутриклеточному накоплению Na и Са, инсулин как митогенный фактор активирует пролиферацию гладко-мышечных клеток сосудов, что ведет к утолщению стенки сосуда.

Роль ИР в патогенезе АГ при СД типа 2
Дедов И.И., Шестакова М.В.
Источник
Гипертония является основным сопутствующим заболеванием у диабетиков. Согласно медицинской статистике — более половины людей с сахарным диабетом имеют проблемы с давлением. Гипертоническая болезнь усложняет лечение и течение основного заболевания, а осложнения могут привести к летальному исходу.
Лечение гипертонии и сахарного диабета — комплексное, и состоит из медикаментов, диеты и перемены образа жизни.
Сахарный диабет и гипертония
При диабете 1 и 2 типа нормальным уровнем АД признается показатель не выше 130/85 мм.рт.ст. Основной же причиной повышенного давления у больных СД становится нарушение обменных процессов. Это приводит к пониженной выработке необходимых гормонов. Большое содержание сахара в крови нарушает целостность и эластичность стенок сосудов. Результат: нарушенный клеточный обмен, накапливание жидкости и натрия, повышение АД и риска возникновения инсульта, острой сердечной недостаточности, инфаркта.
Микроангиопатия клубочком или поражение мелких кровеносных сосудов вызывает плохую работу почек у больных СД 1 типа. Приводит это к выводу белка из организма вместе с мочой. Это объясняет постоянный высокий уровень АД, в результате которого возникает почечная недостаточность. Если же артериальная гипертензия не связана с СД первого типа, то у таких пациентов сохраняются все функции почек.
При втором типе СД пораженные почки приводят к развитию опасных патологий у 20% больных. Рост давления провоцируется развитием инсулинорезистентности — понижением чувствительности тканей к действию инсулина. Чтобы компенсировать это, организм начинает вырабатывать больше инсулина, что ведет к значительному повышению АД. С повышением выработки инсулина возрастает нагрузка на поджелудочную железу. Через несколько лет усиленной работы она перестает справляться с нагрузкой, и в крови еще больше повышается уровень сахара. Это — начало диабета второго типа.

Высокое содержание в крови глюкозы сказывается на повышении АД и развитии гипертонии при диабете следующим образом:
- Происходит активация симпатической нервной системы,
- Почки не справляются с задачей по выведению из организма излишков натрия и жидкости,
- Натрий и кальций оседают в клетках,
- Избыток инсулина провоцирует утолщение стенок сосудов, что приводит к потере эластичности и плохой проходимости.
По мере развития СД просвет в сосудах становится уже, что затрудняет ток крови.
Еще одна опасность — жировые отложения, которыми страдают большинство больных. Жир выделяет в кровь вещества, способствующие повышению артериального давления. Процесс этот называется метаболическим синдромом.
Патогенез гипертонии
К неблагоприятным факторам, повышающим вероятность наступления гипертонического заболевания относят:
- Нехватку микроэлементов, витаминов,
- Отравления,
- Частые стрессы, недосыпания,
- Лишний вес,
- Неправильное питание,
- Атеросклероз.
В группу пациентов повышенного риска входят люди пожилого возраста.
Главной особенностью АГ при сахарном диабете является снижение высокого давления днем, и его повышение в ночное время.
У пациентов с диабетом высокий уровень АД повышает вероятность развития опасных и тяжелых осложнений:
- В 20 раз возрастает риск развития почечной недостаточности, гангрены и неизлечимых язв,
- В 16 раз возрастает риск ухудшения зрения вплоть до слепоты,
- В 5 раз возрастает риск инфаркта и инсульта.
У многих больных, страдающих СД, отмечается осложнение в виде ортостатической гипотонии. Для нее характерны резкие падения АД при вставании (с кровати, дивана, стула и т.д.). Сопровождается это потемнением в глазах, тошнотой, сильными головокружениями и обмороками. Появляется она из-за нарушения сосудистого тонуса, которое называется диабетической нейропатией.
Лечение АГ при сахарном диабете 1 и 2 типа
При наличии высокого АД необходимо проконсультироваться с врачом и не заниматься самолечением. Это может привести к летальному исходу.
Для диабетиков лечащий врач использует:
- Медикаментозные методы: назначаются препараты, понижающие уровень сахара в крови и АД,
- Диеты: при диабете они направлены на уменьшение потребляемой соли, сахара,
- Лечебную физкультуру для борьбы с лишним весом,
- Организацию здорового образа жизни для пациента.
Медикаментозное лечение АГ
Выбор лекарств должен быть тщательным, и основываться на показателях глюкозы, уровне сахара и сопутствующих патологиях. Назначать препарат можно только в соответствии с правилами:
- Он должен понижать АД постепенно на протяжении 2-4 месяцев,
- Лекарство от гипертонии не должно иметь много побочных эффектов и приводить к негативным последствиям,
- Лекарство не должно повышать уровень сахара и ухудшать его баланс,
- Препарат не должен повышать уровень в крови триглецеридора и холестерина,
- Медикамент должен поддерживать нормальную деятельность сердца, почек, сосудов.
Медикаментозные препараты для понижения давления при СД 2 типа подобрать сложнее: нарушенный процесс обмена углеводов дает множество ограничений на использование лекарств.

Диуретики
Группа этих средств помогает организму освободиться от избыточной жидкости, что приводит к понижению АД. Тиазидные препараты (гидрохлортиазид, гипотиазид) при постоянном повышенном уровне сахара снижают риск развития инфаркта и инсульта. Но к их приёму нужно подходить с осторожностью: дневная доза не более 12,5 мг. Передозировка (свыше 50 мг) приведет к значительному повышению уровня сахара. Этот вид препаратов обладает эффектом противодействия возникновению осложнений: почечной недостаточности в острой форме. Противопоказания: почечная недостаточность в хронической стадии. Те же противопоказания и у калийсберегающих препаратов.
Петлевые виды диуретиков назначаются редко: они приводят к диурезу и выводят в больших количествах калий. Это может привести к нарушению сердечного ритма, понижению в крови калиевых ионов. В сочетании с ингибиторами АПФ их прописывают больным с почечной недостаточностью. Лазикс и Фуросемид наиболее безопасны — они не провоцируют повышение сахара, но и не защищают почки.
В случаях, когда гипертония сопровождается 2 типам СД, назначается комбинация мочегонных препаратов с группой ингибиторов АПФ. Одновременный приём мочегонных лекарств и бета блокаторов без наблюдения врача может спровоцировать резкое повышение уровня глюкозы. Для пожилых людей прием диуретиков с бета блокаторами снижает вероятность переломов.
Назначение диуретиков тиазидоподобного вида с ингибиторами АПФ сопровождается мягким мочегонным эффектом, и практически не выводит из организма калий. Небольшая дозировка этих лекарств не оказывает существенного влияния на понижение сахара, протекание ГБ и уровень холестерина.
Ингибиторы
Ингибиторы АПФ (эналаприл) предназначены для блокировки ферментов, способствующих производству ангиотензина II. Этот гормон уменьшает диаметр сосудов и заставляет надпочечники выделять больше альдостерона, задерживающего натрий и жидкость. Применение ингибиторов расширяет просвет в сосудах, в результате чего лишняя жидкость и натрий выводится быстрее. Это приводит к понижению АД.
Ингибиторы АПФ, блокаторы рецепторов ангиотензина II облегчают работу сердечно – сосудистой системы у пациентов с терминальной стадией почечных заболеваний. Прием препаратов приводит к замедлению развития патологий. Лекарства этой группы не провоцируют нарушения липидного обмена, нормализуют чувствительность тканей к воздействию инсулина. Для их безопасного применения необходимо соблюдать бессолевые диеты: ингибиторы АПФ препятствуют выводу калия.
Бета-блокаторы
Бета-блокаторы селективного типа назначаются при гипертонии и диабете, сопровождающимися ишемией и сердечной недостаточностью. Этот препарат также прописывают при 3 степени ГБ. Назначаются бета-блокаторы при анамнезе коронарной болезни сердца и с целью профилактики инфаркта миокарда. При заболеваниях сердечно-сосудистой системы они существенно снижают риск летальных исходов. Группа селективных препаратов понижает АД и не имеет негативных симптомов. Понижение АД происходит за счет блокады β1-рецепторов, и сопровождается снижением частоты и силы сокращений сердца.
Бета-блокаторы неселективной группы при СД не назначаются, поскольку приводят к повышению сахара и вредного холестерина. Блокада β2-рецепторов, которые не находятся в сердце и печени, приводит к отрицательным результатам:
- Приступам астмы,
- Спазмам сосудов,
- Остановке процесса расщепления жиров.
Антагонисты кальция
Эта группа препаратов наиболее эффективна при высоком давлении. Антагонисты калия являются блокаторами кальциевых каналов в мембранах клеток, замедляют поток ионов кальция к клеткам гладких мышц. Длительное применение не вызывает привыкания и ухудшения обмена веществ, это приводит к повышению уровня мочевой кислоты и сахара.
Регулярный прием имеет положительные эффекты:
- Повышение физической выносливости,
- Уменьшение потребности сердечной мышцы в кислороде во время физических нагрузок,
- Блокировка кальциевых каналов, что препятствует проникновение а клетки гладкой мускулатуры жидкости.
- Антагонисты и бета-блокаторы не могут назначаться одновременно.

Противопоказаниями к применению антагонистов является пожилой возраст: чем старше человек, тем больше времени требуется на вывод препарата из организма. Побочными эффектами могут стать резкое падение АД, тахикардия, отеку. Препараты редко назначают при сердечной недостаточности, коронарном заболевании сердца, нестабильной форме стенокардии.
Агонисты
Группа стимуляторов приводит к ослаблению функций симпатической нервной системы, уменьшению числа сердечных сокращений и понижению АД. В результате длительного приема улучшается работа сердца и сосудов. Они противопоказаны при брадикардии, сердечной недостаточности, заболеваниях печени.
Альфа-адреноблокаторы
Применение альфа-адренорецепторы приводит к понижению давления без увеличения частоты сокращений сердца. Противопоказаны они при сердечной недостаточности и ортостатической гипотонии.

Препараты группы альфа – адреноблокаторов часто используют в качестве вспомогательного средства при комбинированном лечении, и как разовое купирование резкого повышения АД. Использование лекарств провоцирует расширение сосудов и сужение вен и артерий, снижение симпатического тонуса. Назначают их в качестве профилактики кризов, инсультов, заболеваний предстательной железы.
Немедикаментозное лечение АГ
Диета
Гипертоникам с СД необходимо придерживаться особого рациона питания. Врачи обычно назначают низкоуглеводные диеты, которые направлены на понижение уровня сахара и нормализацию АД.

Основные правила питания:
- Употребление необходимых витаминов,
- Уменьшение суточной порции соли до 5 г,
- Отказ от жирного,
- Отказ от пищи, богатой натрием (соленая рыба, икра, маслины, сало, копчености и колбасы),
- Прием пищи не менее 5 раз за день,
- Последняя трапеза должна быть за два часа до сна,
- Увеличение в рационе продуктов, содержащих кальций (кунжут, сыр твердых сортов, зелень, орехи, соя, фасоль, фрукты, молочные продукты),
- Употребление нежирных сортов речной и морской рыбы, морепродуктов
- Включение в рацион овощных бульонов,
- Включение в рацион большого количества фруктов, сухофруктов и овощей.
Здоровый образ жизни
Часто больных бывает сложно убедить в эффективности и необходимости здорового образа жизни. В таких случаях пациентам назначается посещение психолога. Стандартным является отказ от курения и алкоголя. Исходя из результатов анализов и общего состояния врач назначает комплекс лечебной физкультуры.

Положительный эффект дают продолжительные прогулки на свежем воздухе и скандинавская ходьба, йога, плавание, занятия лечебной верховой ездой. Людям с СД и гипертонией нужны солнечные и воздушные ванны. Рекомендуется отказаться от работы в ночное и вечернее время, от повышенных эмоциональных и физических нагрузок. Если работа сидячая — в течение дня нужно находить время для занятий простой гимнастикой, чтобы восстановить поток крови в шейном отделе позвоночника. На каждые три часа работы должны быть 20-25 минут отдыха.
Источник


