Артериальное давление перфузионное давление
N.I. Kyrusheva, M.A. Tsaregorodtsva,
T.Ya. Ryabova, V.N. Shlapak
Center of Ophthalmology of FMBA of Russia
Scientific and technical center of radiative and chemical safety and hygiene of FMBA of Russia, Moscow
Purpose: to study peculiarities of ocular perfusion in accordance with vascular dysregulation in patients with normal tension glaucoma (NTG).
Methods: All patients with NTG underwent complete ophthalmologic examination including confocal laser scanning ophthalmoscopy with using of HRT II, optic coherent tomography, standard automatic perimetry, measuring of the perfusion pressure and Doppler mapping for evaluation of the ocular blood flow.
Results and conclusion: 30 patients with initial and developed stage of NTG, age 46–67 years old, were under observation. Control group included 19 healthy subjects, average age – 51±7 years old. Despite the high indices of perfusion pressure in patients with NTG there was significant decrease of the blood flow in the main vessels of optic nerve and this correlated with indices of heart rate variability. The role of primary vascular dysregulation is realized through abnormalities of blood supply autoregulation of the optic nerve.
Одной из наиболее признанных в настоящее время причин развития глаукомы нормального давления (ГНД) является снижение глазной перфузии и, как следствие, ишемии головки зрительного нерва [10]. С. Phelps и J. Corbett впервые указали на еще один возможный механизм развития ГНД, а именно на первичную сосудистую дисрегуляцию (ПСД) [11]. Одним из доказательств, которые приводили эти авторы в пользу данного тезиса, явилось указание на то, что больные ГНД часто страдают мигренью. Позднее это подтвердили и другие авторы [6]. Более того, сочетание ГНД с мигренью повышает риск прогрессирования глаукомной оптиконейропатии (ГОН) в 2,5 раза [9].
Известно, что глазной кровоток при нормальном офтальмотонусе является в определенной мере автономным благодаря существующей ауторегуляции глазной микрогемодинамики [7]. Вместе с тем в условиях ПСД происходит сбой ауторегуляции, и тогда перфузия глаза определяется другими факторами. Было замечено, что у больных с ишемическими заболеваниями зрительного нерва имеется связь регуляции глазного кровотока с показателями сердечного и дыхательного ритмов, иными словами – с параметрами, характеризующими вариабельность сердечного ритма (ВСР) [2].
Анализ ВСР является методом оценки состояния механизмов регуляции физиологических функций в организме человека, в частности общей активности регуляторных механизмов, нейрогуморальной регуляции сердца, соотношения между симпатическим и парасимпатическим отделами вегетативной нервной системы.
Избыточная активность симпатического звена вегетативной нервной системы – одна из возможных причин, ведущих как к первичной сосудистой дисрегуляции, так и к снижению перфузионного давления в сосудах сетчатки, зрительного нерва и хориоидеи.
Проведя исследование вариабельности сердечного ритма у пациентов с ПСД, группой авторов было продемонстрировано, что при ПСД имеются существенные нарушения в балансе симпатического и парасимпатического звеньев вегетативной нервной системы, а именно отмечено явное преобладание симпатической иннервации [5]. В нашем предыдущем исследовании было показано, что у больных ГНД действительно имеет место первичная сосудистая дисрегуляция [4].
Целью настоящей работы явилось изучение особенности глазной перфузии в свете имеющейся первичной сосудистой дисрегуляции при глаукоме нормального давления.
Материалы и методы. Под нашим наблюдением находились 30 пациентов с начальной и развитой стадиями ГНД (основная группа). Возраст больных колебался от 46 до 67 лет, мужчин было 10, женщин – 20. В контрольную группу вошли 19 соматически здоровых лиц (10 мужчин и 9 женщин), не страдающих офтальмопатологией. Средний возраст – 51±7 лет. Из контроля были исключены лица, имеющие в анамнезе признаки первичной или вторичной сосудистой дисрегуляции (мигрень, болезнь Рейно, вазоспазм, нейроциркуляторная дистония). Критериями исключения были также хронические аутоиммунные заболевания, сахарный диабет и любые сопутствующие заболевания, требующие применения стероидных препаратов.
Всем больным проводили полное диагностическое обследование на глаукому, включающее конфокальную лазерную сканирующую офтальмоскопию с использованием HRT II (Heidelberg Engineering), оптическую когерентную томографию на приборе Stratus OCT 3000 (Carl Zeiss Meditec) и стандартную автоматизированную периметрию (Humphrey, Carl Zeiss Meditec) по пороговой программе 30–2.
ГНД диагностировали тем больным, у которых выявлялись признаки ГОН, подтвержденные данными офтальмоскопии и методами визуализации (ДЗН) и слоя нервных волокон сетчатки, а также результатами стандартной автоматизированной периметрии при условии нормального внутриглазного давления (ВГД), что было подтверждено при нескольких измерениях в течение трех дней путем тонометрии по Маклакову, пневмотонометрией и исследованиями на анализаторе биомеханических свойств глаза (ORA, Reichert Inc., США).
У всех обследуемых была проведена оценка функционального состояния сердечно–сосудистой системы до и после пробы с локальным охлаждением на аппаратно–программном комплексе «Ритм–МЭТ», разработанном во ФГУП НТЦ РХБГ ФМБА, Россия по методике, описанной ранее [4]. В качестве провокационного теста в данном исследовании применялась общепринятая проба с локальным охлаждением. Процедура пробы заключалась в следующем. Кисть руки пациента погружалась в холодную воду (+4 °С) с мелкими кусочками льда; дополнительно кисть обкладывалась полиэтиленовыми пакетами со льдом, на 30 секунд. По окончании холодовой пробы вновь проводилась регистрация кардиоинтервалов.
В соответствии с международным стандартом (Heart rate variability. Standards of Mesurement, Physioligical Interpretation and Clinical Use, 1996) [3] учитывались следующие показатели:
– показатель вариабельности сердечного ритма характеризующий суммарный эффект вегетативной регуляции кровообращения (SDNN);
– показатель активности парасимпатического звена вегетативной регуляции (RMSSD);
– показатель абсолютного уровня активности регуляторных систем (TP);
– показатель спектральной мощности дыхательных волн сердечного ритма, отражающий уровень активности дыхательного центра (HF);
– показатель степени преобладания парасимпатического звена регуляции над симпатическим (рNN50);
– индекс вегетативной регуляции (ИВР) – показатель, использующийся для оценки деятельности вегетативной нервной системы. Если ИВР повышен, это свидетельствует об активации симпатической регуляции, если понижен, то парасимпатической регуляции.
В рамках статистического исследования результатов обследования на аппаратно–программном комплексе «Ритм–МЭТ» для каждого из указанных выше показателей определялась величина относительного сдвига показателей после холодовой пробы.
Перфузионное давление определяли по формуле:
Рперф = АД ср –ВГД,
где АД ср = АД диаст + 1/3 (АД сист – АД диаст).
Артериальное давление (АД) измеряли в состоянии покоя в положении сидя. При измерении давления в положении сидя спина имела опору, а средняя точка плеча находилась на уровне сердца (4–е межреберье). Измерение проводилось механическим тонометром фирмы «Адьютор». За 30 мин. перед измерением были исключены прием пищи, курение, физическое напряжение и воздействие холода.
Для оценки кровотока в сосудах глазного яблока и ретробульбарного пространства применяли цветовое допплеровское картирование (ЦДК) и энергетическое картирование (ЭК) при помощи многофункционального ультразвукового диагностического прибора VOLUSON 730 Pro фирмы «Kretz» с использованием линейного датчика частотой от 10 до 16 МГц. Методы ЦДК и ЭК использовали для визуализации кровотока в глазной артерии (ГА), центральной артерии сетчатки (ЦАС), центральной вене сетчатки (ЦВС), медиальных и латеральных задних коротких цилиарных артериях (ЗКЦА), задних длинных цилиарных артериях (ЗДЦА) и регистрации спектра кровотока. Идентификация сосудистых ветвей в ретробульбарном пространстве проводилась по предполагаемому анатомическому прохождению и по направлению тока крови. Поток по направлению к датчику обозначался красным цветом, а от датчика – синим цветом. Направление кровотока также определяли по расположению допплеровской волны выше или ниже изолинии. При помощи допплеровского спектрального анализа идентифицировали пульсирующий артериальный кровоток и более непрерывный или минимально пульсирующий венозный кровоток. Перемещая курсор маркера Доплера, избирательно получали доплеровскую информацию в определенной точке сосуда. При оценке доплеровских характеристик потока в артериях обращали внимание на форму пульсовой волны. В конце исследования регистрировали спектр кровотока и определяли его показатели: максимальную систолическую скорость (Vs), конечную диастолическую скорость (Vd), среднюю скорость в течение сердечного цикла (Vm) и индекс резистентности или периферического сопротивления (RI).
Результаты
Основные результаты настоящего исследования приведены в таблице 1.
Эти результаты показывают, что величины относительного сдвига показателей вариабельности сердечного ритма после холодовой пробы в группе больных ГНД отличаются от аналогичных данных в контроле в сторону сохранения и даже активации симпатического звена нервной системы. Так, увеличение индекса вегетативной регуляции (ИВР) наблюдалось именно у больных ГНД. В контроле, напротив, имело место снижение этого показателя. Об этом же свидетельствует разнонаправленное изменение основного показателя вариабельности сердечного ритма (SDNN) в основной и контрольной группах, а именно снижение в группе больных ГНД и увеличение в контроле. Известно, что уменьшение значения SDNN указывает на смещение баланса вегетативной нервной системы в сторону преобладания симпатической активности, а резкое снижение свидетельствует о значительном напряжении регуляторных систем сердечно–сосудистой системы.
Перфузионное давление (Р перф) при ГНД колебалось от 52 мм рт.ст. до 73 мм рт.ст., средние значения составили 62±4,6 мм рт.ст. В контроле Р перф составило 79±3,5 мм рт.ст. (p<0,05).
Примечательно, что в у больных ГНД перфузионное давление хотя и было достоверно ниже, чем в контроле, тем не менее мы не наблюдали его существенного снижения.
Это можно объяснить тем фактом, что средние значения АД на момент обследования у большинства больных ГНД были в норме (систолическое 118 ±5,0 мм рт.ст., диастолическое 74±4,6 мм рт.ст.), уровень ВГД также находился в пределах нормы (18,6±3,0 мм рт.ст.). Важно подчеркнуть, что суточные колебания АД у больных основной группы колебались в широких пределах: от 85 мм рт.ст. до 135 мм рт.ст. для систолического АД и от 55 мм рт.ст. до 85 мм рт.ст. – для диастолического, у некоторых пациентов отмечалась выраженная гипотония. Однако для расчета Р перф мы брали значения АД на момент проведения исследования ВСР.
Заслуживает внимания тот факт, что была получена высокая корреляция значений перфузионного давления с показателями ВСР. Так, коэффициент корреляции сердечного индекса с Рперф и показателя SDN с Рперф составил 0,63 и 0,75, соответственно (p<0,05). Следует отметить, что уменьшение SDN говорит об усилении симпатической регуляции кровотока. Таким образом, высокая прямая корреляция перфузионного давления с показателем SDN вполне логично объясняет возможность снижения глазной перфузии при повышении активности симпатической регуляции кровотока.
По результатам доплерографии выявлено выраженное снижение максимальной систолической, конечной диастолической скорости кровотока и увеличение индекса резистентности в ЦАС (р<0,001) и ЗКЦА (р<0,05) по сравнению с нормой. Скорость кровотока в центральной артерии сетчатки в систолу при ГНД составила в среднем 5,41±0,08 см/с, в диастолу 1,45±0,12 см/с. В задних коротких цилиарных артериях 8,54±0,12 см/с в систолу и 2,58±0,19 в диастолу. Индекс периферического сопротивления в ЦАС в среднем составлял 0,82±0,09 (р<0,01), в ЗКЦА – 0,78±0,08 (р<0,05).
Примечательно, что показатели глазной гемодинамики существенно коррелировали с параметрами ВСР: так, корреляция параметра SDN с диастолической скоростью кровотока в ЦАС составила 0,9 (p<0,01), аналогичной была корреляция со скоростью кровотока в задних коротких цилиарных артериях как в систолу, так и в диастолу (r=0,93, p<0,01), а с индексом периферического сопротивления в ЗКЦА корреляция составила 0,75 (p<0,01).
Обсуждение результатов
Регуляция глазного кровотока осуществляется на разных уровнях: органном, тканевом, местном (ауторегуляторном). Играют роль клеточный, мембранный и нейрогуморальный механизмы. Зрительный нерв и его сосудистая сеть имеют богатую симпатическую (от шейной симпатической сети) и парасимпатическую (от глазодвигательного нерва) иннервацию. Имеются данные о наличии в сосудистой оболочке глаза нервного сплетения, представленного многочисленными внутренними вегетативными ганглиями, образующими автономную периваскулярную сеть вокруг сосудов хориоидеи. Предполагают, что она играет вазодилаторную функцию, направленную на усиление глазного кровотока при световой нагрузке [8]. По–видимому, вегетососудистые механизмы нарушения трофики зрительного нерва и сетчатки играют существенную роль в физиологии и патофизиологии глаза. Вазоконстрикция происходит на фоне преобладания симпатоадреналовых влияний на артериолы и капилляры, а также вследствие снижения активности парасимпатических влияний на артериолы.
Некоторые авторы предполагают, что существует связь вегетативной нейрогенной и миогенной регуляции общего и глазного микрокровотока у больных ГНД. Экспериментально выявлено, что при этом играют роль локальные причины, приводящие к спазму глазных артерий. Так, П.П. Бакшинским и соавт. было отмечено, что у больных с нормальным ВГД может иметь место спастический тип глазной микроциркуляции. При этом нарушение глазного микрокровотока связано с изменениями работы пассивных механизмов регуляции общего микрокровотока, определяемых сердечными и дыхательными ритмами [1].
Полученные нами данные указывают на тот факт, что у больных ГНД несмотря на высокие цифры перфузионного давления, рассчитанного по традиционно применяемой формуле, отмечалось существенное угнетение глазного кровотока в основных сосудах, питающих зрительный нерв, и это снижение коррелировало с показателями вариабельности сердечного ритма.
Кроме того, настоящее исследование подтвердило роль ПСД в патогенезе ГНД. Известно, что сама по себе ПСД не приводит к дефициту кровообращения в ДЗН, но реализуется через нарушение ауторегуляции [10]. Можно предположить, что именно сбой ауторегуляции явился причиной сниженного кровотока у обследованных пациентов.
Таким образом, проведенное исследование продемонстрировало важность определения показателей вариабельности сердечного ритма у больных ГНД, сдвиг которых после проведения холодового теста, свидетельствует об активации симпатического звена регуляции кровотока и является более информативным, чем определение перфузионного давления.
Источник
Церебральное
перфузионное давление (ЦПД) —
это
разница между средним артериальным
давлением
(АДср) и ВЧД (или церебральным венозным
давлением).
Если церебральное венозное давление
значительно
превышает ВЧД, то ЦПД равно разнице
между АДср и церебральным венозным
давлением.
В
физиологических условиях ВЧД незначительно
отличается от церебрального венозного
давления,
поэтому принято считать, что ЦПД = =
АДср — ВЧД. В норме церебральное
перфузионное
давление составляет 100 мм рт. ст. и зависит
главным
образом от АДср, потому что ВЧД у
здорового
человека не превышает 10 мм рт. ст.
При
выраженной внутричерепной гипертензии
(ВЧД
> 30 мм рт. ст.) ЦПД и MK
могут
значительно
снижаться даже при нормальном АДср. ЦПД
<
50 мм рт. ст. проявляется замедлением
ритма на ЭЭГ,
ЦПД в пределах от 25 до 40 мм рт. ст. —
изолинией
на ЭЭГ, а при устойчивом снижении ЦПД
менее
25 мм рт. ст. возникает необратимое
повреждение
мозга.
2. Ауторегуляция мозгового кровообращения
В
головном мозге, так же как в сердце и
почках, даже значительные колебания АД
не оказывают существенного
влияния на кровоток. Сосуды мозга
быстро реагируют на изменение ЦПД.
Снижение
ЦПД вызывает вазодилатацию сосудов
мозга, увеличение
ЦПД — вазоконстрикцию. У здоровых людей
MK
остается
неизменным при колебаниях АДср
в пределах от 60 до 160 мм рт. ст. (рис. 25-1).
Если
АДср выходит за границы этих значений,
то ауторегуляция
MK
нарушается.
Увеличение АДср до
160 мм рт. ст. и выше вызывает повреждение
ге-матоэнцефалического
барьера (см. ниже), чреватое
отеком мозга и геморрагическим инсультом.
При
хронической артериальной гипертонии
кривая
ауторегуляции мозгового кровообращения
(рис.
25-1) смещается
вправо, причем
сдвиг затрагивает
и нижнюю, и верхнюю границы. При
артериальной
гипертонии снижение АД до обычных
значений (меньше измененной нижней
границы)
приводит к уменьшению MK,
в
то время как высокое
АД не вызывает повреждения мозга.
Длительная
гипотензивная терапия может восстановить
ауторегуляцию мозгового кровообращения
в
физиологических границах.
Существуют
две теории ауторегуляции мозгового
кровообращения — миогенная и
метаболическая.
Миогенная теория объясняет механизм
ауторегуляции
способностью гладкомышечных клеток
церебральных
артериол сокращаться и расслабляться
в зависимости от АДср. Согласно
метаболической
теории, тонус церебральных артериол
зависит
от потребности мозга в энергетических
субстратах.
Когда потребность мозга в энергетических
субстратах
превышает их доставку, в кровь выделяются
тканевые метаболиты, которые вызывают
церебральную
вазодилатацию и увеличение MK.
Этот
механизм опосредуют ионы водорода (их
роль
в церебральной вазодилатации описана
раньше),
а также другие вещества — оксид азот
(NO),
аденозин,
простагландины и, возможно, градиенты
ионной
концентрации.
3. Внешние факторы
Парциальное
давление CO2и
O2в
крови
Рис.
25-1. Ауторегуляция
мозгового кровообращения
Парциальное
давление CO2
в
артериальной крови (PaCO2)
—
наиболее важный внешний фактор, влияющий
на MK.
MK
прямо
пропорционален PaCO2
в
пределах от 20 до ЗОммрт. ст. (рис.
25-2). Увеличение PaCO2
на
1 мм рт. ст. влечет за собой мгновен-
ное повышение MK
на 1-2 мл/100 г/мин,
уменьшение
PaCO2
приводит
к эквивалентному снижению
MK.
Этот
эффект опосредуется через рН
цереброспинальной
жидкости и вещества мозга. Поскольку
CO2,
в
отличие от ионов, легко проникает,
через гематоэнцефалический барьер, то
на MK
влияет
именно острое изменение PaCO2,
а
не концентрации
HCO3‘.
Через 24-48 ч после
начала гипо-
или гиперкапнии развивается компенсаторное
изменение концентрации HCO3″
в
спинномозговой
жидкости. При выраженной гипервентиляции
(PaCO2
<
20 мм рт. ст.) даже у здоровых людей на
ЭЭГ появляется картина, аналогичная
таковой при повреждении головного
мозга. Острый метаболический ацидоз
не оказывает значительного влияния
на MK,
потому
что ион водорода (H+)
плохо
проникает через гематоэнцефалический
барьер. Что
касается PaO2,
то
на MK
оказывают
воздействие
только его значительные изменения. В
то время
как гипероксия снижает MK
не
более чем на 10 %, при тяжелой гипоксии
(PaO2
<
50 мм рт. ст.) MK
увеличивается
в гораздо большей степени (рис. 25-2).
Температура
тела
Изменение
MK
составляет
5-7 % на 1 0C.
Гипотермия
снижает CMRO2и MK,
в то время как
гипер-термия оказывает обратный эффект.
Уже при 20
0C
на
ЭЭГ регистрируют изолинию, но дальнейшее
уменьшение температуры позволяет еще
сильнее снизить
потребление кислорода мозгом. При
температуре выше 42 0C
потребление кислорода
мозгом
также снижается, что, по-видимому,
обусловлено повреждением нейронов.
Вязкость
крови
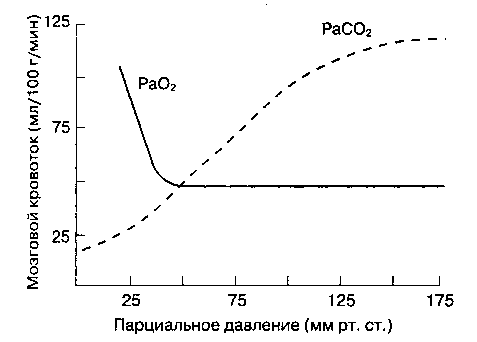
Рис.
25-2. Влияние
PaO2
и
PaCO2Ha
мозговой
кровоток
У здоровых людей вязкость
крови не оказывает значительного влияния
на MK. Вязкость
крови
в
наибольшей степени зависит от гематокрита,
поэтому снижение
гематокрита уменьшает вязкость и
увеличивает MK.
К сожалению, помимо
этого благоприятного эффекта, снижение
гематокрита имеет и отрицательную
сторону: оно уменьшает кислородную
емкость крови и, соответственно, доставку
кислорода. Высокий гематокрит, например
при тяжелой полицитемии, увеличивает
вязкость крови и снижает MK.
Исследования
показали, что для лучшей доставки
кислорода к мозгу гематокрит должен
составлять 30-34 %.
Вегетативная
нервная система
Внутричерепные
сосуды иннервируются симпатическими
(вазоконстрикторными), парасимпатическими
(вазодилатирующими) и нехолинергическими
неадренергическими
волокнами; нейротрансмитте-ры
в последней группе волокон — серотонин
и вазо-активный
интестинальный пептид. Функция
вегетативных
волокон сосудов мозга в физиологических
условиях неизвестна,
но продемонстрировано их участие
при некоторых патологических состояниях.
Так,
импульсация по симпатическим волокнам
pis
верхних
симпатических ганглиев может значительно
сузить крупные мозговые сосуды и
уменьшить MK.
Вегетативная
иннервация мозговых сосудов играет
важную роль в возникновении церебрального
вазоспазма после Ч MT
и
инсульта.
Гематоэнцефалический
барьер
Между эндотелиальными
клетками мозговых сосудов практически
отсутствуют поры. Малочисленность
пор — основная морфологическая
особенность
гематоэнцефалического
барьера. Липидный
барьер проницаем для жирорастворимых
веществ, но значительно ограничивает
проникновение ионизированных частиц
и крупных молекул.
Таким
образом, проницаемость гематоэнцефалического
барьера для молекулы какого-либо вещества
зависит от ее размера, заряда, липо-фильности
и степени связывания с белками крови.
Углекислый газ,
кислород и липофильные вещества (к
которым относят большинство анестетиков)
легко проходят через гематоэнцефалический
барьер,
в то время как для большинства ионов,
белков и крупных
молекул (например, маннитола) он
практически
непроницаем.
Вода
свободно проникает через гематоэнцефалический
барьер по механизму объемного тока, а
перемещение
даже небольших ионов затруднено (время
полу выравнивания для натрия составляет
2-4 ч). В результате
быстрые изменения концентрации
электролитов плазмы (а значит, и
осмолярности)
вызывают преходящий
осмотический градиент между плазмой и
мозгом. Остро возникшая гипер-тоничность
плазмы приводит к перемещению воды из
вещества мозга в кровь. При острой
гипотонич-ности плазмы, наоборот,
происходит перемещение воды
из крови в вещество мозга. Чаще всего
равновесие
восстанавливается без особых последствий,
но
в ряде случаев существует опасность
быстро развивающихся
массивных перемещений жидкости, чреватых
повреждением мозга. Следовательно,
значительные
нарушения концентрации натрия или
глюкозы в плазме нужно устранять медленно
(см. гл.
28). Маннитол, осмотически активное
вещество, которое в физиологических
условиях не пересекает гематоэнцефалический
барьер, вызывает устойчивое
уменьшение содержания воды в мозге и
часто используется
для уменьшения объема мозга.
Целостность
гематоэнцефалического барьера нарушают
тяжелая артериальная гипертензия,
опухоли
мозга, ЧМТ, инсульт, инфекции, выраженная
гиперкапния, гипоксия, устойчивая
судорожная активность. При
этих состояниях перемещение
жидкости через гематоэнцефалический
барьер определяется не осмотическим
градиентом, а гидростатическими
силами.
Цереброспинальная
жидкость
Цереброспинальная
жидкость находится
в желудочках
и цистернах головного мозга, а также в
суб-арахноидальном
пространстве ЦНС. Главная функция
цереброспинальной жидкости — защита
мозга
от травмы.
Большая часть цереброспинальной
жидкости вырабатывается в сосудистых
сплетениях желудочков
мозга (преимущественно в боковых).
Некоторое
количество образуется непосредственно
в
клетках эпендимы желудочков, а совсем
небольшая часть — из жидкости,
просачивающейся через периваскулярное
пространство сосудов мозга (утечка
через гематоэнцефалический барьер). У
взрослых образуется 500 мл цереброспинальной
жидкости в сутки
(21 мл/ч), в то время как объем цереброспинальной
жидкости составляет только 150
мл. Из боковых желудочков цереброспинальная
жидкость через межжелудочковые отверстия
(отверстия
Монро) проникает в третий желудочек,
откуда
через водопровод мозга (сильвиев
водопровод)
попадает в четвертый желудочек. Из
четвертого
желудочка через срединную апертуру
(отверстие Мажанди)
и боковые апертуры (отверстия Люшка)
цереброспинальная жидкость поступает
в
мозжечково-мозговую (большую) цистерну
(рис. 25-3), а оттуда — в субарахноидальное
пространство головного и спинного
мозга, где и цир-
кулирует
до тех пор, пока не всасывается в
грануляциях паутинной оболочки
больших полушарий. Для образования
цереброспинальной жидкости необходима
активная секреция натрия в сосудистых
сплетениях.
Цереброспинальная жидкость изото-нична
плазме, несмотря на более низкую
концентрацию
калия, бикарбоната и глюкозы. Белок
поступает в
цереброспинальную жидкость только из
перивас-кулярных
пространств, поэтому его концентрация
очень
невелика. Ингибиторы карбоангидразы
(аце-тазоламид),
кортикостероиды, спиронолактон,
фу-росемид,
изофлюран и вазоконстрикторы уменьшают
выработку цереброспинальной жидкости.
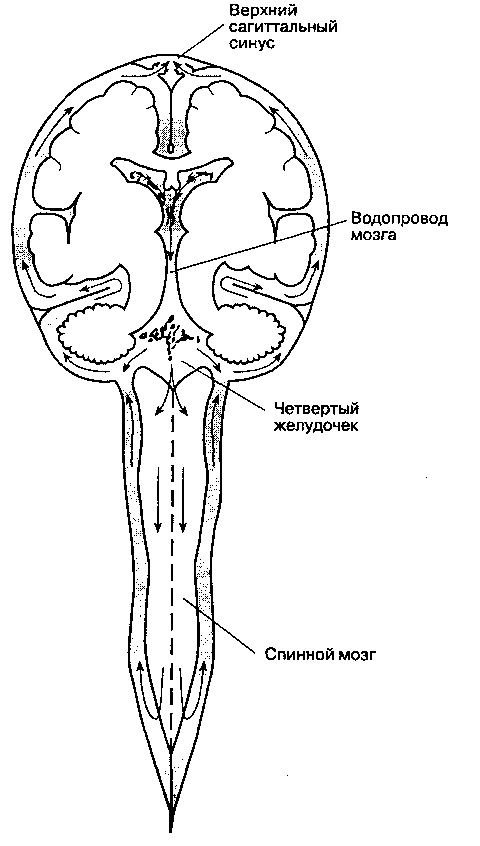
Рис.
25-3. Циркуляция
цереброспинальной жидкости в центральной
нервной системе. (С разрешения. Из:
De-GrootJ.,
ChusidJ. G. Correlative
Neuro anatomy,
21st
ed. Appleton &
Lange,
1991.)
Цереброспинальная
жидкость всасывается в грануляциях
паутинной оболочки, откуда попадает в
венозные синусы. Небольшое количество
всасывается
через лимфатические сосуды мозговых
оболочек
и периневральные муфты. Обнаружено, что
всасывание
прямо пропорционально ВЧД и обратно
пропорционально церебральному венозному
давлению; механизм этого явления неясен.
Поскольку
в головном и спинном мозге нет
лимфатических
сосудов, всасывание цереброспинальной
жидкости — основной путь возвращения
белка из
интерстициальных и периваскулярных
пространств
мозга обратно в кровь.
Внутричерепное
давление
Череп
представляет собой жесткий футляр с
нерастягивающимися
стенками. Объем полости черепа неизменен,
его занимает вещество мозга (80 %), кровь
(12
%) и цереброспинальная жидкость (8 %).
Увеличение
объема одного компонента влечет за
собой равное
по величине уменьшение остальных, так
что ВЧД не
повышается. ВЧД
измеряют с помощью датчиков, установленных
в боковом желудочке или на поверхности
полушарий головного мозга; в норме его
величина
не превышает 10 мм рт. ст. Давление
цереброспинальной жидкости, измеренное
при люмбальной пункции
в положении больного лежа на боку,
достаточно
точно соответствует величине ВЧД,
полученной
с помощью внутричерепных датчиков.
Растяжимость
внутричерепной системы определяют,
измеряя прирост ВЧД при увеличении
внутричерепного
объема. Вначале увеличение внутричерепного
объема хорошо компенсируется (рис.
25-4), но
после достижения определенной точки
ВЧД резко
возрастает. Основные компенсаторные
механизмы включают:
(1) смещение цереброспинальной жидкости
из полости черепа в субарахноидальное
пространство
спинного мозга; (2) увеличение всасывания
цереброспинальной жидкости; (3) уменьшение
образования цереброспинальной жидкости;
(4) уменьшение
внутричерепного объема крови (главным
образом за счет венозной).
Податливость
внутричерепной системы неодинакова
в разных участках мозга, на нее влияют
АД и PaCO2.
При повышении АД
механизмы ауторе-гуляции
вызывают вазоконстрикцию сосудов мозга
и снижение внутричерепного объема
крови. Артериальная
гипотония, наоборот, приводит к
ва-зодилатации сосудов мозга и увеличению
внутричерепного
объема крови. Таким образом, благодаря
ауторегуляции просвета сосудов MK
не изменяется при
колебаниях АД. При повышении PaCO2
на
1 мм рт. ст. внутричерепной объем крови
увеличивается
на 0,04 мл/100 г.
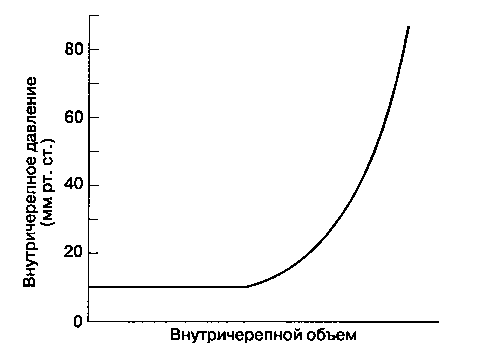
Рис.
25-4. Растяжимость
внутричерепной системы в норме
Концепцию
растяжимости внутричерепной системы
широко используют в клинической практике.
Растяжимость
измеряют при введении стерильного
физиологического раствора во
внутрижелудоч-ковый
катетер. Если после инъекций 1 мл раствора
ВЧД увеличивается
более чем на 4 мм рт. ст., то растяжимость
считают значительно сниженной. Снижение
растяжимости свидельствует об истощении
механизмов компенсации и служит
прогностическим
фактором уменьшения MK
при
дальнейшем прогрессировании внутричерепной
гипертензии.
Устойчивое повышение ВЧД может вызвать
катастрофическую дислокацию и вклинение
различных участков мозга. Выделяют
следующие
виды повреждений (рис. 25-5): (1) ущемление
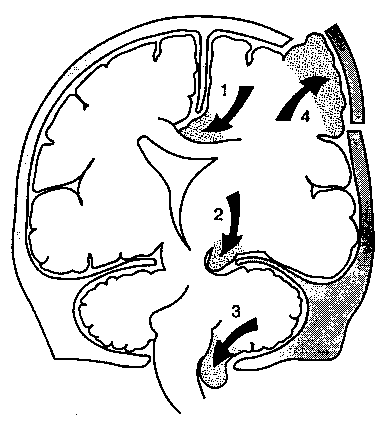
Рис.
25-5. Дислокации
головного мозга. (С разрешения. Из:
Fishman
R. A. Brain edema. New England J. Med., 1975;
293:706.)
поясной извилины серпом
мозга; (2) ущемление крючка
наметом мозжечка; (3) сдавленна
продолговатого мозга при вклинении
миндалин мозжечка в большое затылочное
отверстие; (4) выпячивание вещества
мозга через дефект черепа.
Влияние
анестетиков
и
вспомогательных средств
наЦНС
Подавляющее большинство
общих анестетиков благоприятно
воздействует на ЦНС, снижая биоэлектрическую
активность мозга. Катаболизм углеводов
уменьшается, в то время как запасы
энергии в виде АТФ, АДФ и фосфокреатина
возрастают. Оценить эффект отдельного
препарата очень сложно, потому что на
него накладывается действие других
средств, хирургическая стимуляция,
растяжимость внутричерепной системы,
АД и PaCO2.
Например, гипокапния
и предварительное
введение тиопентала предотвращают
увеличение MK
и ВЧД при использовании
кетамина pi
ингаляционных
анестетиков. В этом разделе описано
действие каждого препарата в отдельности.
Итоговая табл. 25-1 позволяет оценить и
сравнить
влияние анестетиков и вспомогательных
средств на ЦНС. В
разделе также обсуждается роль
миорелаксантов и средств, оказывающих
воздействие
на сосудистый тонус.
Ингаляционные
анестетики
Источник

